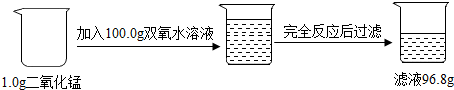
题目内容
8.水是生命之源,下列有关水的说法正确的是( )| A. | 水是常用的溶质 | |
| B. | 水汽化时分子大小发生了变化 | |
| C. | 正常雨水呈酸性 | |
| D. | 电解水得到氢气与氧气的质量比为2:1 |
分析 A、根据水能溶解很多种物质分析;
B、根据水汽化时的变化分析;
C、根据二氧化碳能与水化合生成了碳酸分析;
D、根据电解水实验的现象和结论分析.
解答 解:A、水能溶解很多种物质,水是常用的溶剂,故A错误;
B、水汽化时,水分子的间隔变大了,水分子大小没有发生变化,故B错误;
C、由于二氧化碳能与水化合生成了碳酸,所以,正常雨水呈酸性,故C正确;
D、电解水得到氢气与氧气的质量比为1:8,故D错误.
故选C.
点评 本题主要考查了有关水的知识,属于课本中的基础知识,难度不大,加强有关水的知识的归纳和学习有利于解答本题.

练习册系列答案
相关题目
19.氢氧化钠固体及溶液在空气中很容易发生变质生成碳酸钠.
(1)甲同学在实验室里发现一瓶敞口放置的氢氧化钠溶液,对其变质情况进行了如下探究.
【猜想与假设】该氢氧化钠溶液已部分变质.
【实验与结论】
【拓展探究】甲同学又尝试通过实验除去该氢氧化钠溶液中含有的碳酸钠,方案如下:
向该溶液中加入适量氢氧化钙,反应后,经过滤操作,即可除去该氢氧化钠溶液中含有的杂质.
(2)乙同学在实验室里发现少量部分变质的氢氧化钠固体,尝试通过实验测定其中碳酸钠的质量分数.
【设计和进行实验】乙同学设计了如图所示的实验装置(铁架台、铁夹等固定用装置已略去,碱石灰是固体氢氧化钠和生石灰的混合物),取10.0g待测样品,进行实验.
实验步骤如图:
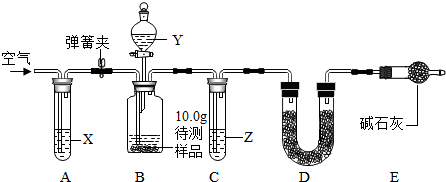
a.连接好装置,并检查气密性;
b.打开弹簧夹,缓缓通入一段时间空气;
c.称量装置D的质量为83.4g;
d.关闭弹簧夹,慢慢滴加Y溶液,至不再产生气泡为止;
e.打开弹簧夹,再次缓缓通入一段时间空气;
f.再次称量装置D的质量为84.5g.
【交流讨论】
①试剂X、Y、Z依次最适宜选用C(选填字母).
A.氢氧化钠溶液 浓盐酸 浓硫酸 B.澄清石灰水 稀盐酸 稀硫酸
C.氢氧化钠溶液 稀硫酸 浓硫酸 D.浓硫酸 稀硫酸 氢氧化钠溶液
②步骤e中通入空气的作用是将B中产生的二氧化碳全部赶到D装置中.
③若没有装置C或E,则会导致测定结果偏大(选填“偏大”、“偏小”或“无影响”)
【数据处理】根据实验中测得的有关数据,计算部分变质的氢氧化钠固体中碳酸钠的质量分数是26.5%.
(1)甲同学在实验室里发现一瓶敞口放置的氢氧化钠溶液,对其变质情况进行了如下探究.
【猜想与假设】该氢氧化钠溶液已部分变质.
【实验与结论】
| 实验步骤 | 实验现象 | 实验结论 |
| a.取少量该溶液于一支试管中,加入足量氯化钙溶液 | 有白色沉淀生成 | 该氢氧化钠溶液已变质 |
| b.将步骤a所得的液体过滤,取滤液于另一支试管中,滴加无色酚酞试液 | 酚酞试液变红 | 该氢氧化钠溶液已部分变质 |
向该溶液中加入适量氢氧化钙,反应后,经过滤操作,即可除去该氢氧化钠溶液中含有的杂质.
(2)乙同学在实验室里发现少量部分变质的氢氧化钠固体,尝试通过实验测定其中碳酸钠的质量分数.
【设计和进行实验】乙同学设计了如图所示的实验装置(铁架台、铁夹等固定用装置已略去,碱石灰是固体氢氧化钠和生石灰的混合物),取10.0g待测样品,进行实验.
实验步骤如图:

a.连接好装置,并检查气密性;
b.打开弹簧夹,缓缓通入一段时间空气;
c.称量装置D的质量为83.4g;
d.关闭弹簧夹,慢慢滴加Y溶液,至不再产生气泡为止;
e.打开弹簧夹,再次缓缓通入一段时间空气;
f.再次称量装置D的质量为84.5g.
【交流讨论】
①试剂X、Y、Z依次最适宜选用C(选填字母).
A.氢氧化钠溶液 浓盐酸 浓硫酸 B.澄清石灰水 稀盐酸 稀硫酸
C.氢氧化钠溶液 稀硫酸 浓硫酸 D.浓硫酸 稀硫酸 氢氧化钠溶液
②步骤e中通入空气的作用是将B中产生的二氧化碳全部赶到D装置中.
③若没有装置C或E,则会导致测定结果偏大(选填“偏大”、“偏小”或“无影响”)
【数据处理】根据实验中测得的有关数据,计算部分变质的氢氧化钠固体中碳酸钠的质量分数是26.5%.
16.为测定某AgNO3溶液的溶质质量分数,某兴趣小组的同学分五次进行了实验,每次向100g AgNO3溶液加入一定量的铜粉,充分反应后过滤、洗涤、干燥.测得相关数据如下:
(1)上表中数据a的值为0.8;
(2)上述实验中第四(填序号)次实验铜粉与AgNO3溶液恰好完全反应;
(3)计算该AgNO3溶液的溶质质量分数;
(4)第五次实验所得滤液的质量为96.2g.
| 实验序号 | 一 | 二 | 三 | 四 | 五 |
| 加入铜粉质量/g | 0.4 | a | 1.2 | 1.6 | 2 |
| 所得滤渣质量/g | 1.35 | 2.7 | 4.05 | 5.4 | 5.8 |
(2)上述实验中第四(填序号)次实验铜粉与AgNO3溶液恰好完全反应;
(3)计算该AgNO3溶液的溶质质量分数;
(4)第五次实验所得滤液的质量为96.2g.
3.X是合成维生素A的重要原料.工业上用物质甲和乙在一定条件下反应生成物质丙和X,甲、乙和丙的微观示意图见下表.
该反应中甲、乙、丙的质量比为23:17:1.下列判断不正确的是( )
| 物质 | 甲 | 乙 | 丙 | X | |
| 微观 示意图 |  |  |  | ? |  |
| A. | X属于化合物 | |
| B. | 该反应方程式中乙与丙的化学计量数之比为2:3 | |
| C. | 物质X中含三种元素 | |
| D. | 该反应为置换反应 |
13.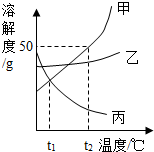 甲、乙、丙三种不含结晶水的固体物质的溶解度曲线如图所示,下列说法中正确的是( )
甲、乙、丙三种不含结晶水的固体物质的溶解度曲线如图所示,下列说法中正确的是( )
 甲、乙、丙三种不含结晶水的固体物质的溶解度曲线如图所示,下列说法中正确的是( )
甲、乙、丙三种不含结晶水的固体物质的溶解度曲线如图所示,下列说法中正确的是( )| A. | t2℃时将50g甲物质放入50g水中,充分搅拌后得到100g甲溶液 | |
| B. | t1℃时将接近饱和的丙溶液升温可转化为饱和溶液 | |
| C. | 乙中混有少量的甲,要提纯乙通常可采用冷却热饱和溶液的方法 | |
| D. | 分别将t2℃时三种物质的饱和溶液降温到t1℃,甲溶液中析出的晶体最多 |
20.保护环境,节约资源,从我做起.下列做法不符合这一理念的是( )
| A. | 使用降解塑料 | B. | 推广乙醇汽油 | ||
| C. | 减少燃煤使用 | D. | 废旧电池掩埋在土壤中 |
18.在我市生产的一种大米中富含有硒,这里的“硒”应理解为( )
| A. | 单质 | B. | 分子 | C. | 元素 | D. | 原子 |