题目内容
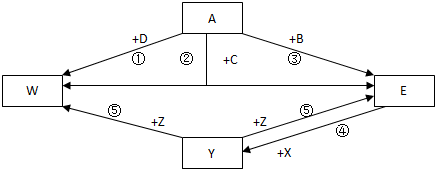
12.某白色固体A,在一定条件下可以分解成B、C两种物质,其中B为无色气体,C为白色固体,将点燃的细铁丝放入B中,剧烈燃烧,火星四射,生成黑色固体D,若向A中加入一种暗紫色固体E,开始时产生气体速度较为缓慢,接着产生气体的速度大加快,而且产生的气体的量也大大增加,经验定,这种暗紫色固体E在反应过程中也能生成无色气体B;请根据上述信息回答下列问题:(1)由此可以推断:A氯酸钾;D四氧化三铁;E高锰酸钾;(填物质名称).
(2)写出下列反应的文字表达式:
A→B:氯酸钾$\stackrel{二氧化锰}{→}$氯化钾+氧气;
铁+B→D:铁+氧气$\stackrel{点燃}{→}$四氧化三铁.
(3)向A中加入一种暗紫色固体E,发现开始时产生气体速度较为缓慢,接着产生气体的速度大大加快,其原因是高锰酸钾分解产生的二氧化锰作为氯酸钾分解的催化剂.反应完全后,产生气体的量比同质量的A(不加固体E)完全反应产生的气体多,其原因是:高锰酸钾分解也能产生氧气.
分析 根据将点燃的细铁丝放入B中,剧烈燃烧,火星四射,生成黑色固体D可知B是氧气,D是四氧化三铁;某白色固体A,在一定条件下可以分解成B、C两种物质,其中B为无色气体,C为白色固体可知A是氯酸钾,C是氯化钾;若向A中加入一种暗紫色固体E,开始时产生气体速度较为缓慢,接着产生气体的速度大加快,而且产生的气体的量也大大增加,经验定,这种暗紫色固体E在反应过程中也能生成无色气体B,可知暗紫色的固体E是高锰酸钾,高锰酸钾分解产生锰酸钾、二氧化锰和氧气,其中二氧化锰可以作为氯酸钾分解的催化剂,据此分析.
解答 解:将点燃的细铁丝放入B中,剧烈燃烧,火星四射,生成黑色固体D可知B是氧气,D是四氧化三铁;某白色固体A,在一定条件下可以分解成B、C两种物质,其中B为无色气体,C为白色固体可知A是氯酸钾,C是氯化钾;若向A中加入一种暗紫色固体E,开始时产生气体速度较为缓慢,接着产生气体的速度大加快,而且产生的气体的量也大大增加,经验定,这种暗紫色固体E在反应过程中也能生成无色气体B,可知暗紫色的固体E是高锰酸钾,高锰酸钾分解产生锰酸钾、二氧化锰和氧气,其中二氧化锰可以作为氯酸钾分解的催化剂,因此:
(1)A是氯酸钾,D是四氧化三铁,E是高锰酸钾,故填:氯酸钾;四氧化三铁;高锰酸钾;
(2)A→B是氯酸钾在二氧化锰的作用下分解产生氯化钾和氧气,铁+B→D是铁和氧气点燃产生四氧化三铁;故填:氯酸钾$\stackrel{二氧化锰}{→}$氯化钾+氧气;铁+氧气$\stackrel{点燃}{→}$四氧化三铁;
(3)因为高锰酸钾分解产生锰酸钾、二氧化锰和氧气,其中二氧化锰作为氯酸钾分解的催化剂,可以加快反应的速率;故填:高锰酸钾分解产生的二氧化锰作为氯酸钾分解的催化剂;高锰酸钾分解也能产生氧气.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后进行验证即可.

 名校课堂系列答案
名校课堂系列答案| A. | 猜想假设 | B. | 收集证据 | C. | 设计实验 | D. | 得出结论 |
| A. | Mg>Al>Fe | B. | Al>Mg>Fe | C. | Fe>Mg>Al | D. | Mg═Al═Fe |
| A. | 铝加氧气等于氧化铝 | |
| B. | 铝跟氧气在点燃的条件下,反应生成氧化铝 | |
| C. | 每9份铝在8份氧气中燃烧生成17份氧化铝 | |
| D. | 4个铝原子和6个氧原子等于2个氧化铝分子 |
| A. | X2Y | B. | XY | C. | X3Y2 | D. | XY2 |