题目内容
现将10g铜锌(Cu﹣Zn)合金放入到一定质量的稀硫酸中恰好完全反应,过滤得到100g溶质质量分数为16.1%的溶液.据此请完成下列问题:
(1)生产氢气 g;
(2)稀硫酸中H2SO4的质量是 g;
(3)合金中铜的质量分数是多少?
0.2 9.8
解:设生成氢气的质量为x,稀硫酸中H2SO4的质量为y,黄铜样品中锌的质量为z,
Zn+H2SO4=ZnSO4 +H2↑
65 98 161 2
z y 100g×16.1% x
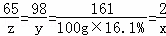 x=0.2g y=9.8g z=6.5g
x=0.2g y=9.8g z=6.5g
合金中铜的质量分数=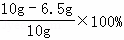 =35%
=35%
答:合金中铜的质量分数是35%.

 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案在实验室中化学兴趣小组的同学发现了一瓶敞口放置的Ca(OH)2粉末状试剂.他们对该试剂进行了定量实验分析:称取试剂19.8g放入锥形瓶中,加入30.2g的水,充分振荡,再向锥形瓶中依次滴加25g盐酸充分反应.测得部分数据与图象如下.请根据有关信息回答问题.
| 第1次 | 第2次 | 第3次 | 第4次 | 第5次 | 第6次 | |
| 加入盐酸的质量(g) | 25 | 25 | 25 | 25 | 25 | 25 |
| 锥形瓶中物质的质量(g) | 75 | 100 | a | 150 | 172.8 | 197.8 |
(1)a的数值为 ,兴趣小组的同学通过实验,得出该试剂已部分变质的结论,其依据是(通过实验数据和图象做出你的分析) . .
(2)b的数值为 .
计算该试剂中氢氧化钙的质量分数(写出计算过程,结果保留一位小数).
铝合金的生产与销售是潍坊市一条重要的产业链,为测定某种铝铜合金中铝的质量分数,探究小组进行了如下实验:
| 实验编号 | 铝铜合金的质量(g) | 加入稀硫酸的质量(g) | 生成H2的质量(g) |
| 实验1 | 30 | 392 | 2 |
| 实验2 | 30 | 588 | 3 |
| 实验3 | 30 | 600 | 3 |
(1)所用稀硫酸溶质的质量分数为 .
(2)该铝铜合金中铝的质量分数是多少?
如图所示,A-H都是初中化学中常见的物质,已知:常温下,A是黑色固体单质,B是黑色固体化合物,D为红色固体单质,F为Fe2O3,它们的转化关系如图所示。 按要求完成下列各题:
按要求完成下列各题:
|









 A C E
A C E
|
|



 B D G
B D G
(1)写出下列物质的化学式: C ,E 。
(2)写出上图中① ② ③反应的化学方程式:
① ② ;③ 。
(3)反应的①③基本反应类型都是 ,反应②的基本反应类型是 。
 生石灰。将滴管甲中的水滴入烧杯丙中,可观察到气球鼓起,一段时间后装置恢复原状。利用所学化学知识解释气球鼓起的原因是 ,烧杯丙中发生反应的化学方程式为 。
生石灰。将滴管甲中的水滴入烧杯丙中,可观察到气球鼓起,一段时间后装置恢复原状。利用所学化学知识解释气球鼓起的原因是 ,烧杯丙中发生反应的化学方程式为 。