题目内容
10.下列描述属于氧气化学性质的是( )| A. | 通常情况下,氧气是无色、无味的气体 | |
| B. | 通过低温加压,可使氧气液化为淡蓝色的液体 | |
| C. | 氧气可供给动植物呼吸 | |
| D. | 氧气是一种性质比较活泼的气体,能氧化许多物质 |
分析 根据物理性质与化学性质的定义和本质区别进行分析判断,物理性质是不需要发生化学变化就能表现出来的性质,化学性质是在化学变化中表现出来的性质,二者的本质区别:是否通过化学变化表现出来;据此结合氧气的化学性质进行分析解答.
解答 解:A、通常情况下,氧气是无色、无味的气体,不需要发生化学变化就能表现出来,为物理性质,故选项错误.
B、通过低温加压,可使氧气液化为淡蓝色的液体,不需要发生化学变化就能表现出来,为物理性质,故选项错误.
C、氧气可供给动植物呼吸是氧气的用途,故选项错误.
D、氧气一种性质比较活泼的气体,能氧化许多物质,氧气具有氧化性,需要发生化学变化就能表现出来,为化学性质,故选项正确.
故选:D.
点评 本题难度不大,掌握氧气的化学性质、物理性质与化学性质本质区别(是否通过化学变化表现出来)是正确解答本题的关键.

练习册系列答案
相关题目
20.某同学对下列4个实验都设计了两种方案,其中两种方案都合理的是( )
| 选项 | A | B | C | D |
| 实验 目的 | 除去CuSO4溶液中少量的H2SO4 | 除去NaOH溶液中少量的Na2CO3 | 鉴别O2和CO2气体 | 除去CO中少量的CO2 |
| 方案1 | 加入足量的Fe粉,过滤 | 滴入适量的石灰水,过滤 | 用带火星的木条 | 点燃 |
| 方案2 | 加入足量的CuO,过滤 | 滴入适量的CaCl2溶液,过滤 | 用紫色石蕊溶液 | 通入足量的NaOH溶液 |
| A. | A | B. | B | C. | C | D. | D |
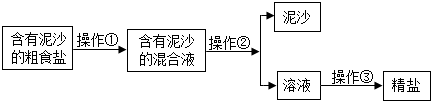
1.学习了二氧化锰对过氧化氢分解有催化作用的知识后,某同学想:氧化铜(CuO)能否起到类似二氧化锰的催化剂作用呢?于是进行了以下探究.
【猜想】:
Ⅰ、氧化铜不是催化剂、也不参与反应,反应前后质量和化学性质不变;
Ⅱ、氧化铜参与反应产生氧气,反应前后质量和化学性质发生了改变;
Ⅲ、氧化铜是反应的催化剂,反应前后质量和化学性质不变.
【实验】
用天平称量0.2g氧化铜(CuO),取5mL5%的过氧化氢溶液于试管中,进行如图1实验:
(1)填写下表:
(2)步骤①的目的是与步骤③对照.
(3)过氧化氢能被氧化铜催化分解放出氧气的文字表达式为过氧化氢$\stackrel{氧化铜}{→}$水+氧气.
(4)同学通过查阅资料得知,过氧化氢在70℃以上会较快分解产生氧气.为了验证加热过氧化氢也可以产生氧气,同学们选择如图2装置(气密性良好)进行实验.实验中观察到试管内产生大量气泡,但将带火星的木条放在导管口没有复燃,可能的原因是放出的氧气中含有较多的水蒸气,同学分析原因后,采用了排水法收集气体,再检验,证明加热双氧水也可产生氧气.
【猜想】:
Ⅰ、氧化铜不是催化剂、也不参与反应,反应前后质量和化学性质不变;
Ⅱ、氧化铜参与反应产生氧气,反应前后质量和化学性质发生了改变;
Ⅲ、氧化铜是反应的催化剂,反应前后质量和化学性质不变.
【实验】
用天平称量0.2g氧化铜(CuO),取5mL5%的过氧化氢溶液于试管中,进行如图1实验:

(1)填写下表:
| 步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 | |
| 溶液中有气泡放出, 带火星的木条复燃. | 称量的氧化铜的质量 仍为0.2g | 溶液中有气泡放出 带火星的木条复燃 | 猜想Ⅰ、Ⅱ不成立;猜想Ⅲ成立. | |
(3)过氧化氢能被氧化铜催化分解放出氧气的文字表达式为过氧化氢$\stackrel{氧化铜}{→}$水+氧气.
(4)同学通过查阅资料得知,过氧化氢在70℃以上会较快分解产生氧气.为了验证加热过氧化氢也可以产生氧气,同学们选择如图2装置(气密性良好)进行实验.实验中观察到试管内产生大量气泡,但将带火星的木条放在导管口没有复燃,可能的原因是放出的氧气中含有较多的水蒸气,同学分析原因后,采用了排水法收集气体,再检验,证明加热双氧水也可产生氧气.
2.在化学实验中从试剂瓶中取出的药品使用后有剩余,对这些药品的处置方法合理的是( )
| A. | 带出实验室自己处理 | B. | 放回原试剂瓶 | ||
| C. | 放入指定的容器内 | D. | 投入通向下水道的水槽中 |
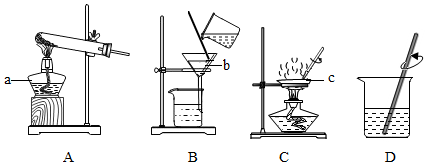
 A、B两图分别表示硫、铁丝在氧气中燃烧示意图
A、B两图分别表示硫、铁丝在氧气中燃烧示意图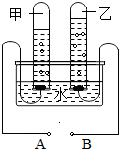 如图是水电解实验示意图.
如图是水电解实验示意图.