题目内容
14.氯酸钾和高锰酸钾是初中常见的化学物质,在生活中也应用广泛,如高锰酸钾俗称“灰锰氧”,在生活中常用作消毒剂等.根据所学知识回答:(1)氯酸钾和高锰酸钾在物质分类中属于盐(填“氧化物”、“酸”、“碱”或“盐”).
(2)氯酸钾和高锰酸钾都可以制取氧气,是因为它们的组成中都含有相同氧元素.
(3)氯酸钾和高锰酸钾阳离子对应的碱都是KOH(填化学式).
(4)高锰酸钾在一定条件下能与浓盐酸反应,反应的化学方程式如下:2KMnO4+16HCl(浓)═2KCl+2MnCl2+5□↑+8H2O则“□”中的化学式为Cl2,其中锰元素的化合价由+7价变为+2价.
分析 (1)根据酸、碱、盐的定义分析:氧化物是由两种元素组成并且一种元素是氧元素的化合物;电离时生成的阳离子都是氢离子的化合物是酸,电离时生成的阴离子都是氢氧根离子的化合物是碱,由金属离子和酸根离子组成的化合物是盐;
(2)根据氯酸钾和高锰酸钾的组成进行分析;
(3)根据氯酸钾和高锰酸钾的粒子构成及碱的概念进行分析;
(4)根据质量守恒定律及化合物中元素的化合价规律进行分析解答.
解答 解:(1)氯酸钾和高锰酸钾是由钾离子和酸根离子组成的化合物,属于盐;
(2)酸钾和高锰酸钾都可以制取氧气,是因为它们的组成中都含有相同的元素--氧元素;
(3)氯酸钾和高锰酸钾的阳离子都是钾离子,根据碱的概念,钾离子对应的碱是:氢氧化钾,化学式为:KOH;
(4)根据方程式和质量守恒定律,参加反应的氯原子有16个,反应后也应有16个,而在已知的生成物中共有6个,所以方框内的生成物应是氯气,其化学式为:Cl2; 设KMnO4中锰元素的化合价为x,则+1+x+(-2)×4=0,x=+7;设MnCl2中锰元素的化合价为y,则y+(-1)×2=0,y=+2;
故答案为:(1)盐;(2)氧元素;(3)KOH; (4)Cl2;+7;+2.
点评 本题考查物质的组成、分类及质量守恒定律的运用,题目难度不大,可依据已有知识进行解答.

练习册系列答案
相关题目
4.请结合图示实验装置,有下列几种说法:
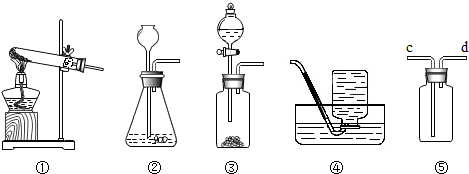
a.利用装置①④制氧气,水槽中出现气泡时收集O2
b.利用双氧水和MnO2制取O2,选用装置③可以控制反应的速率
c.利用装置②④组合可制取并收集CO2
d.利用石灰石和稀盐酸制取CO2时,选用③⑤,收集时气体由d端进入
上述四种说法中,正确的个数有( )

a.利用装置①④制氧气,水槽中出现气泡时收集O2
b.利用双氧水和MnO2制取O2,选用装置③可以控制反应的速率
c.利用装置②④组合可制取并收集CO2
d.利用石灰石和稀盐酸制取CO2时,选用③⑤,收集时气体由d端进入
上述四种说法中,正确的个数有( )
| A. | 1 个 | B. | 2 个 | C. | 3 个 | D. | 4 个 |
5.除去下列各组物质中的杂质,所用试剂和方法均正确的是( )
| 物质 | 杂质 | 除杂所用的试剂和方法 | |
| A | CaO | CaCO3 | 加入适量的稀盐酸,蒸发 |
| B | CuO | Cu | 加入过量的稀硫酸、再过滤 |
| C | NaOH溶液 | Ca(OH)2 | 先加入适量的Na2CO3溶液,再过滤 |
| D | KCl溶液 | CuCl2 | 加入氢氧化钾溶液至不再产生沉淀,过滤 |
| A. | A | B. | B | C. | C | D. | D |
2.下列实验操作,先后顺序正确的一项是( )
| A. | 检查装置气密性时,先用双手紧贴试管外壁,再将导管的一端浸入水中 | |
| B. | 使用H2O2溶液和MnO2制氧气时,先将药品装入装置,然后检查装置的气密性 | |
| C. | 使用滴管时,先用手指捏紧橡胶乳头,然后把滴管伸入试剂瓶中,放开手指,吸入液体试剂 | |
| D. | 实验室制取、收集氧气时,先将导气管伸入盛满水的集气瓶,再给试管加热 |
9.某学生为了验证锌、银、铜三种金属的活动性顺序,设计了五个实验,下列实验组合不能验证锌、银、铜三种金属活动性顺序的是( )
①将Zn、Cu分别放入稀盐酸中; ②将Ag放入Cu(NO3)2溶液中;③将Cu放入AgNO3溶液中;④将Cu放入ZnSO4溶液中;⑤将Zn放入AgNO3溶液中.
①将Zn、Cu分别放入稀盐酸中; ②将Ag放入Cu(NO3)2溶液中;③将Cu放入AgNO3溶液中;④将Cu放入ZnSO4溶液中;⑤将Zn放入AgNO3溶液中.
| A. | ①② | B. | ①③ | C. | ②④ | D. | ①⑤ |
19.某环保小组监测到一湿法冶铜厂排放的废水中含有硫酸和硫酸铜两种污染物,为测定该废水中各污染物的含量,给冶铜厂提供处理废水的参考,环保小组的同学进行了以下实验.取废水200g,向其中加入溶质质量分数为20%的氢氧化钠溶液.测得生成沉淀的质量与所加入的氢氧化钠溶液的质量关系如下表:
根据所得数据分析和计算:
(1)向200g该废水中加入足量的氢氧化钠溶液产生沉淀的质量为19.6g.
(2)200g该废水中硫酸铜的溶质质量分数.
(3)200g该废水中硫酸的溶质质量为9.8g.
(4)另取同样的200g该废水,向其中加入17.1%的Ba(OH)2溶液.请你画出加入Ba(OH)2溶液的质量与产生沉淀的质量的关系图.(在答题卡的坐标中作图,并标出曲线折点的坐标)
| 加入的氢氧化钠溶液的质量/g | 40 | 80 | 120 | 160 |
| 生成沉淀的质量/g | 0 | 9.8 | 19.6 | 19.6 |
(1)向200g该废水中加入足量的氢氧化钠溶液产生沉淀的质量为19.6g.
(2)200g该废水中硫酸铜的溶质质量分数.
(3)200g该废水中硫酸的溶质质量为9.8g.
(4)另取同样的200g该废水,向其中加入17.1%的Ba(OH)2溶液.请你画出加入Ba(OH)2溶液的质量与产生沉淀的质量的关系图.(在答题卡的坐标中作图,并标出曲线折点的坐标)
6.下图所示的变化中,属于化学变化的是( )
| A. |  分馏石油 分馏石油 | B. |  净化水 | ||
| C. |  蒸发食盐水 | D. |  燃烧红磷 |
3.化学在生活中有广泛的应用,下列说法错误的是( )
| A. | 活性炭可除去水中的异味但不能降低水的硬度 | |
| B. | 使用农药、化肥对人类有利也有弊 | |
| C. | 商家用甲醛溶液浸泡海产品保鲜对顾客有益 | |
| D. | 食用加铁酱油、加碘食盐等可补充人体健康必需的化学元素 |