��Ŀ����
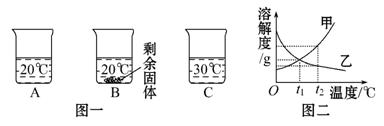
ijͬѧ��ⶨij100g����������Һ�����������������������ȡ10g�������̷����ձ��У������ù���������Һȫ�����룬��ͬʱ���õ�����ƽ���������������ö��������ʾ��
| ��Ӧʱ��/min | 0 | 1 | 2 | 3 | 4 | 5 | 6 |
| �ձ�����ʢ����������/g | 335.70 | 334.30 | 334.00 | 333.50 | 333.00 | 332.50 | 332.50 |
��1���Է�����100g����������Һ��ȫ��Ӧ����������������Ϊ������
��2������100g����������Һ�й���������������Ϊ���٣���д��������̣�
��3��������÷����ⶨ������ܻ�ƫ���ԭ��������д��һ�㼴�ɣ���
�� ������
��1�����������غ㶨�ɣ���Ӧǰ��ʱ��Ϊ0ʱ�ձ�����ʢ��������������ȫ��Ӧ���ٲ�������ʱ��Ϊ5minʱ�ձ�����ʢ�����������IJ��Ϊ��Ӧ�ų�����������������
��2�����ݹ��������ڶ������̴��·ֽ�����ˮ�������Ļ�ѧ����ʽ�������������������������Ӧ���Ĺ����������������200g��Һ���������ʵ��������������������ʹ����������������Һ������200g�������������������㹫ʽ���м��㼴�ɣ������������Һ�����ʵ�����������
��3������������������ƫ��˵��������ʵ�����ƫ����н��
���
�⣺��1��ȡ10g�������̷����ձ��м�������200g����������Һ�������ٷų�����ʱ���ձ�����ʣ�����ʵ�������Ϊ332.50g����Ӧǰ��������Ϊ�ų���������������Ӧ������������=335.70g��332.50g=3.2g��
�ʴ�Ϊ��3.2g��
��2����������������Ϊx
2H2O2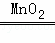 2H2O+O2��
2H2O+O2��
68 32
x 3.2g
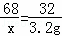
x=6.8g
����������Һ����������=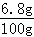 ��100%=6.8%
��100%=6.8%
�𣺹���������Һ��������������Ϊ6.8%��
��3��������������ƫ��˵��������ʵ�����ƫ�����Կ����Dzⶨ�����з�Ӧ���ձ�����ʢ����������ƫС������ⶨ�����з�Ӧ���ձ�����ʢ����������ƫС��

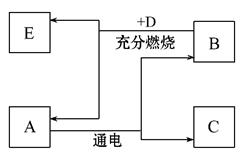
ů������һ�ַ�����Ʒ����ͼ��ʾ��ů�����е���Ҫ�ɷ�����Щ�����ȵ�ԭ����ʲô��
��1��С��̽����ů�����е���Ҫ�ɷ���ʲô�������ڰ�װ�����������еķ�ĩ�����ֳʺ�ɫ��
��������롿�ú�ɫ��ĩ���ܺ���̿�ۡ����ۡ��������̡�����ͭ��������
�����е�һ�ֻ��֣�
��������֤��������������ɫ��ĩ�����ֱ�������
���������ϡ��������������д��ԣ��ܱ�����������
���ó����ۡ��ú�ɫ��ĩ���ܺ��С�����
������ʵ�顿
| ʵ���� | ʵ����� | ʵ������ |
| �� | ȡ��ɫ��ĩ������ϡ���� | ���岿���ܽ⣬�����ݲ�������Һ����ɫ |
| �� | ȡʵ��ٵIJ������գ����ڱ�Ϳ�� ����ʯ��ˮ��С�ձ������Ϸ� | ����ʯ��ˮ����� |
��ʵ��ٿ�֪���ú�ɫ��ĩ�϶����������϶�����������д��ʵ��ٵĻ�ѧ��Ӧ����ʽ������
��ʵ��ڿ�֪���ú�ɫ��ĩ�϶���������
��2��С��˼����ů����Ϊʲô�ᷢ�ȣ�
���������ϡ�ů�����е������ڿ����з����˻��������������ų��������ɴ˿ɼ������ǿ������û�ѧ��Ӧ�ų������������پ�һ����������
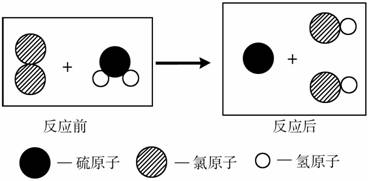
��3���������û�ѧ��Ӧ�����ԡ�����

ʵ������ ����������Һ�Ͷ���������ȡ������ʵ�������������±���
����������Һ�Ͷ���������ȡ������ʵ�������������±���
| ���巢��װ�������ʵ�������/g | |
| ��Ӧǰ | 35.6 |
| ��Ӧ�� | 34.8 |
��1����Ӧ�ж������̵�������__________ ___________��
___________��
 ��2����Ӧ��������������Ϊ_______________g�������ȷ��0.1g����ͬ����
��2����Ӧ��������������Ϊ_______________g�������ȷ��0.1g����ͬ����
��3������μӷ�Ӧ�Ĺ��������������