题目内容
四只烧杯分别盛有 ①稀盐酸 ②饱和的石灰水 ③少量酚酞试液 ④少量石蕊试液中的两种(如图所示),据实验回答问题:
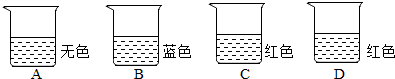
(1)B由 (填序号)混合而成.
(2)向A、D中加入碳酸钙固体有气泡产生,反应的化学方程式为 .
(3)欲使C中溶液浑浊,可采用的方法有 (填序号,下同),若采用上述方法中的 还可观察到溶液红色消失.
①升温 ②降温 ③通入CO2 ④加入CaO.

(1)B由
(2)向A、D中加入碳酸钙固体有气泡产生,反应的化学方程式为
(3)欲使C中溶液浑浊,可采用的方法有
①升温 ②降温 ③通入CO2 ④加入CaO.
考点:酸的化学性质,生石灰的性质与用途,书写化学方程式、文字表达式、电离方程式
专题:常见的酸 酸的通性
分析:(1)根据已有的知识进行分析,石蕊试液在酸性溶液中为红色,在碱性溶液中为蓝色,酚酞试液在碱性溶液中为红色,在酸性或中性溶液中为无色;由于B中溶液为蓝色,故B中溶液呈碱性,可能是氢氧化钙;
(2)由于A中溶液为无色,故A中溶液呈酸性或中性,由题中信息可知A为稀盐酸,由D中溶液为红色,向A、D中加入碳酸钙固体有气泡产生,故D中溶液呈酸性;
石灰石和稀盐酸制取二氧化碳,产生氯化钙、水和二氧化碳解答;
(3)由C中溶液为红色,根据(2)D中溶液呈酸性,可知C中溶液碱性,故C是饱和的石灰水,由于氢氧化钙的溶解度随温度的升高而降低,二氧化碳能和氢氧化钙反应生成碳酸钙沉淀,氧化钙和水反应生成氢氧化钙,会析出氢氧化钙溶质解答.
(2)由于A中溶液为无色,故A中溶液呈酸性或中性,由题中信息可知A为稀盐酸,由D中溶液为红色,向A、D中加入碳酸钙固体有气泡产生,故D中溶液呈酸性;
石灰石和稀盐酸制取二氧化碳,产生氯化钙、水和二氧化碳解答;
(3)由C中溶液为红色,根据(2)D中溶液呈酸性,可知C中溶液碱性,故C是饱和的石灰水,由于氢氧化钙的溶解度随温度的升高而降低,二氧化碳能和氢氧化钙反应生成碳酸钙沉淀,氧化钙和水反应生成氢氧化钙,会析出氢氧化钙溶质解答.
解答:解:
(1)由于B中溶液为蓝色,故B中溶液呈碱性,可能是氢氧化钙和少量石蕊试液;
(2)由于A中溶液为无色,故A中溶液呈酸性或中性,由题中信息可知A为稀盐酸,由D中溶液为红色,向A、D中加入碳酸钙固体有气泡产生,故D中溶液呈酸性;
石灰石和稀盐酸制取二氧化碳,产生氯化钙、水和二氧化碳,反应的化学反应方程式;CaCO3+2HCl═CaCl2+H2O+CO2↑;
(3)由C中溶液为红色,根据(2)D中溶液呈酸性,可知C中溶液碱性,故C是饱和的石灰水,由于氢氧化钙的溶解度随温度的升高而降低,二氧化碳能和氢氧化钙反应生成碳酸钙沉淀,氧化钙和水反应生成氢氧化钙,会析出氢氧化钙溶质,故选①③④,二氧化碳能消耗氢氧化钙,碱性消失,溶液红色消失.
答案:
(1)②④
(2)CaCO3+2HCl═CaCl2+H2O+CO2↑;
(3)①③④③
(1)由于B中溶液为蓝色,故B中溶液呈碱性,可能是氢氧化钙和少量石蕊试液;
(2)由于A中溶液为无色,故A中溶液呈酸性或中性,由题中信息可知A为稀盐酸,由D中溶液为红色,向A、D中加入碳酸钙固体有气泡产生,故D中溶液呈酸性;
石灰石和稀盐酸制取二氧化碳,产生氯化钙、水和二氧化碳,反应的化学反应方程式;CaCO3+2HCl═CaCl2+H2O+CO2↑;
(3)由C中溶液为红色,根据(2)D中溶液呈酸性,可知C中溶液碱性,故C是饱和的石灰水,由于氢氧化钙的溶解度随温度的升高而降低,二氧化碳能和氢氧化钙反应生成碳酸钙沉淀,氧化钙和水反应生成氢氧化钙,会析出氢氧化钙溶质,故选①③④,二氧化碳能消耗氢氧化钙,碱性消失,溶液红色消失.
答案:
(1)②④
(2)CaCO3+2HCl═CaCl2+H2O+CO2↑;
(3)①③④③
点评:本题考查了常见物质成分的推断,完成此题,可以依据物质的性质进行.要注意根据反应的实验现象进行判断.

练习册系列答案
相关题目
下列有关金属的说法错误的是( )
| A、金属具有金属光泽,常温下金属都是固体 |
| B、生铁和钢是含碳量不同的铁合金,其中生铁的含碳量大于钢的含碳量 |
| C、不能用铁桶盛放农药波尔多液 |
| D、金属的化学性质越活泼,其发现和使用的年代一般越晚 |
下列各组物质,能在pH=1的溶液中大量共存,且形成无色溶液的是( )
| A、NaCl Na2SO4 Na2CO3 |
| B、NaNO3 NaCl CuSO4 |
| C、NaNO3 HCl Na2SO4 |
| D、NaOH BaCl2 Na2SO4 |
 如图,灯焰处a为
如图,灯焰处a为 如图是水分解的示意图.请回答:
如图是水分解的示意图.请回答: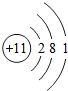 ,C元素是地壳中含量最多的元素,D元素组成的单质是最清洁的燃料,则元素A为
,C元素是地壳中含量最多的元素,D元素组成的单质是最清洁的燃料,则元素A为


