题目内容
8.已知某地石灰石的主要成分为CaCO3,所含杂质不溶于水,也不参加反应.化学兴趣小组为测定石灰石中CaCO3的质量分数,进行了以下实验:称石灰石样品两份,分别放入大烧杯中,第一个烧杯中加入50g稀盐酸,第二个烧杯中放入100g同样的稀盐酸,充分反应至不再有气泡产生时称量残留物质量,有关数据如表.| 各物质的质量 | 第一个烧杯 | 第二个烧杯 |
| 石灰石样品质量 | 12g | 12g |
| 稀盐酸质量 | 50g | 100g |
| 烧杯残留物质量 | 58.7g | 107.6g |
| 产生的CO2质量 | 3.3g | 4.4g |
(1)两个烧杯中产生CO2的质量(填入如表空格中);
(2)石灰石样品中CaCO3的质量分数.(写出计算过程,结果精确到0.1%)
分析 (1)根据质量守恒定律可以计算出二氧化碳的质量;
(2)根据在化学方程式中二氧化碳的质量,可以计算碳酸钙的质量;
解答 解:
(1)第一个烧杯稀盐酸完全反应,产生二氧化碳质量:12g+50g-58.7g=3.3克;
第二个烧杯石灰石样品完全反应,产生二氧化碳质量:12g+100g-107.6g=4.4克;
(2)设石灰石中CaCO3的质量为X,
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 4.4g
$\frac{100}{x}=\frac{44}{4.4g}$
x═10g
石灰石中CaCO3的质量分数=$\frac{10g}{12g}$×100%=83.3%
答案:
(1)第一个烧杯产生二氧化碳质量3.3g;第二个烧杯产生二氧化碳质量4.4g;
(2)石灰石样品中CaCO3的质量分数83.3%
点评 本题主要考查了学生分析图表数据,解决问题的能力,以及据方程式计算的能力.

练习册系列答案
相关题目
18.化学学习小组做实验时记录了下列实验现象,其中正确的是( )
| A. | 在过氧化氢溶液中加入少量二氧化锰,立即生成了大量氧气 | |
| B. | 在含有石蕊的氢氧化钠溶液中逐滴加入稀硫酸时,溶液颜色由蓝色逐渐变成紫色 | |
| C. | 硫在空气中燃烧,发出明亮的蓝紫色火焰,产生刺激性气味的气体 | |
| D. | 打开盛有浓盐酸的瓶盖,瓶口产生大量白色烟雾 |
19.下列叙述正确的是( )
| A. | 用汽油和洗涤剂分别除去衣服上的油污,两者去污原理不同 | |
| B. | 由不同种元素组成的物质一定是混合物 | |
| C. | 铝比铁具有更好的抗腐蚀性能,是因为铁比铝更活泼 | |
| D. | 某物质能与碱反应生成盐和水,则该物质一定是酸 |
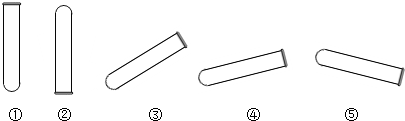
3.下列实验操作正确的是( )
| A. |  取用液体 | B. | 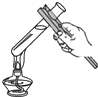 加热液体 | C. |  稀释浓硫酸 | D. |  蒸发食盐水 |
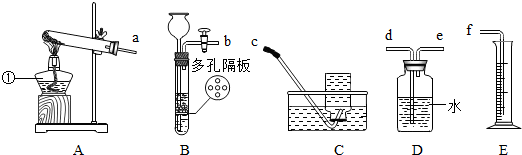
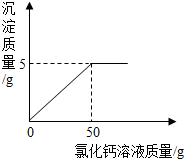 为检验某久置的氢氧化钠样品是否变质,现称取变质的氢氧化钠样品10g,配制成溶液,再向其中加入CaCl2溶液,产生沉淀.反应时CaCl2溶液与沉淀的质量关系如图所示.请解决以下问题:
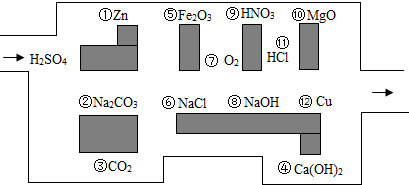
为检验某久置的氢氧化钠样品是否变质,现称取变质的氢氧化钠样品10g,配制成溶液,再向其中加入CaCl2溶液,产生沉淀.反应时CaCl2溶液与沉淀的质量关系如图所示.请解决以下问题: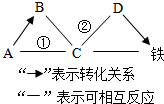 A、B、C、D分别为氧化铁、盐酸、氢氧化钙、碳酸钙中的一种,它们之间的反应或转化关系如图(部分物质和反应条件已略去),则A的化学式为Ca(OH)2;反应①所属的基本反应类型为复分解反应,反应②化学方程式为Fe2O3+6HCl=2FeCl3+3H2O.
A、B、C、D分别为氧化铁、盐酸、氢氧化钙、碳酸钙中的一种,它们之间的反应或转化关系如图(部分物质和反应条件已略去),则A的化学式为Ca(OH)2;反应①所属的基本反应类型为复分解反应,反应②化学方程式为Fe2O3+6HCl=2FeCl3+3H2O.