题目内容
13.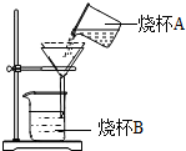 过滤操作如图所示,指出其中的错误之处:
过滤操作如图所示,指出其中的错误之处:(1)未用玻璃棒引流;
(2)滤纸高出漏斗边缘;
(3)滤纸未紧贴漏斗内壁;
(4)漏斗下端尖嘴未紧靠烧杯B的内壁.
分析 过滤操作要求做到“一贴两低三靠”即:一贴,滤纸紧贴头都内壁;两低,滤纸低于漏斗,液面低于滤纸边沿;三靠,玻璃棒末端要与滤纸三层处相靠,烧杯嘴要与玻璃棒中部相靠,漏斗下端口要与烧杯内壁相靠.
解答 解:图示的过滤操作存在多处错误:未用玻璃棒引流,会在倒入液体时使滤纸破损;滤纸高出漏斗边缘,会导致液体流出漏斗;滤纸未紧贴漏斗内壁,液体从滤纸与漏斗之间流过,过滤不彻底;漏斗下端尖嘴未紧靠烧杯B的内壁,液体流速小且会溅起.
故答案为:(1)未用玻璃棒引流:(2)滤纸高出漏斗边缘;(3)滤纸未紧贴漏斗内壁;(4)漏斗下端尖嘴未紧靠烧杯B的内壁.
点评 本题难度不大,熟悉各种仪器的用途及使用注意事项、掌握常见化学实验基本操作的注意事项是解答此类试题的关键.

练习册系列答案
 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案
相关题目
11.下列三幅图都来自课本,都是和水相关的,结合图形,指出下列说法中叙述正确的是( )
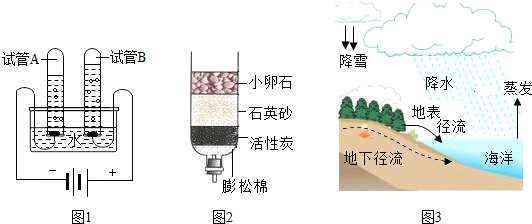

| A. | 图2得到的水是纯净物 | |
| B. | 三幅图中水的化学性质不同 | |
| C. | 在图1的变化过程中分子种类发生改变 | |
| D. | 图3中水的状态前后不会改变 |
4.甲、乙、丙三位同学对实验室制备氧气的条件进行如下探究实验.
(1)甲为探究催化剂的种类对氯酸钾分解速度的影响,设计以下对比实验:
Ⅰ.将3.0gKClO3与1.0gMnO2均匀混合加热
Ⅱ.将xgKClO3与1.0gCuO均匀混合加热
其Ⅱ中x的值应该是3.0;
(2)乙探究了影响双氧水分解速度的某种因素.实验数据记录如下:
本实验中,测量O2体积的装置是C(填编号):
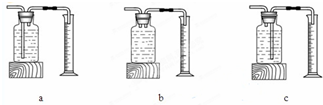
实验结论:在相同条件下,双氧水的浓度越大,双氧水分解得越快.
(3)丙同学也对影响过氧化氢分解速率的影响作了猜想和验证,你认为他的猜想是与温度有关.(答案合理即可)
(1)甲为探究催化剂的种类对氯酸钾分解速度的影响,设计以下对比实验:
Ⅰ.将3.0gKClO3与1.0gMnO2均匀混合加热
Ⅱ.将xgKClO3与1.0gCuO均匀混合加热
其Ⅱ中x的值应该是3.0;
(2)乙探究了影响双氧水分解速度的某种因素.实验数据记录如下:
| 双氧水的质量 | 双氧水的浓度 | MnO2的质量 | 相同时间内产生O2体积 | |
| Ⅰ | 50.0g | 1% | 0.1g | 9mL |
| Ⅱ | 50.0g | 2% | 0.1g | 16mL |
| 50.0g | 4% | 0.1g | 31mL |

实验结论:在相同条件下,双氧水的浓度越大,双氧水分解得越快.
(3)丙同学也对影响过氧化氢分解速率的影响作了猜想和验证,你认为他的猜想是与温度有关.(答案合理即可)
8.下列操作或现象与分子对应的特性不一致的选项是( )
| 选项 | 操作、现象或事实 | 分子的特性 |
| A | 气体容易被压缩 | 分子间有间隙 |
| B | 一滴水中含有1.67×1021个水分子 | 分子很小 |
| C | 物体热胀冷缩 | 分子可变大或变小 |
| D | 墙内开花墙外香 | 分子在不停地运动 |
| A. | A | B. | B | C. | C | D. | D |
2.下列有关说法正确的是( )
| A. | 纯碱、火碱与稀盐酸均能发生中和反应 | |
| B. | 部分变质的氢氧化钠溶液滴入少量的稀盐酸,可能无气泡 | |
| C. | 石灰水、氢氧化钠溶液敞口放置均会因为发生化学变化而使其溶液质量增多 | |
| D. | 某无色溶液的成分可能为:KCl、K2CO3、H2SO4 |
3.规范的操作是化学实验成功的保障.下列实验操作的先后顺序正确的是( )
| A. | 制取二氧化碳时,先加稀盐酸,再加大理石 | |
| B. | 用排水法收集氧气收满时,先把集气瓶从水中拿出,再盖上玻璃片 | |
| C. | 洗涤加热高锰酸钾制氧气的试管时,先冷却,再用水洗 | |
| D. | 用胶头滴管吸取液体时,先把滴管伸入液体中,再挤压胶头 |
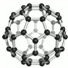 C60的模型如图所示,每个碳原子和相邻的3个碳原子以小棍结合.若要搭建一个这样的模型,需要代表碳原子的小球60个,需要代表化学键的连接小球的小棍90根.
C60的模型如图所示,每个碳原子和相邻的3个碳原子以小棍结合.若要搭建一个这样的模型,需要代表碳原子的小球60个,需要代表化学键的连接小球的小棍90根.