题目内容
实验表明浓硫酸与焦炭在加热的条件下能发生反应,某化学小组对该反应中生成的气体展开了科学探究.【提出问题】产生的气体的成分是什么?
【查阅资料】①SO2可使澄清石灰水变浑浊; ②SO2可使品红溶液的红色褪去,而CO2不能;③SO2可与酸性的KMnO4溶液反应使其褪色,而CO2不能;④CuSO4为白色粉末,遇水可生成蓝色的胆矾.
【分析讨论】经过分析讨论,大家认为产生的气体可能是H2O、CO2、SO2中的两种或三种.
【提出猜想】猜想1:产生的气体是CO2和H2O;
猜想2:产生的气体是H2O和SO2;
猜想3:产生的气体是
猜想4:产生的气体是H2O,CO2和SO2
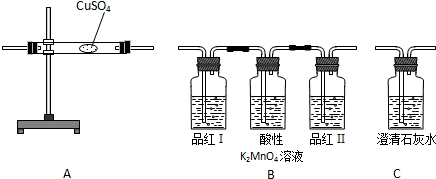
【实验探究】小组同学通过对下图装置进行组装并开展探究
【结论】浓硫酸与焦炭在加热的条件下反应的方程式是
【反思】小明取久置的浓硫酸和焦炭进行该实验,但发现两者没有发生反应,可能的原因是
分析:猜想3:从大家认为产生的气体可能是H2O、CO2、SO2中的两种或三种考虑;
【结论】根据反应物和反应条件以及质量守恒定律写出化学反应式;
【反思】从久置的浓硫酸可能吸收了空气中的水分考虑.
【结论】根据反应物和反应条件以及质量守恒定律写出化学反应式;
【反思】从久置的浓硫酸可能吸收了空气中的水分考虑.
解答: 解:
解:
猜想3:大家认为产生的气体可能是H2O、CO2、SO2中的两种或三种,除猜想1和猜想2外,还应有SO2和CO2.
故答案为:SO2和CO2;
【结论】浓硫酸与焦炭在加热的条件下反应,根据质量守恒定律可知,生成物质要有C、H、O、S几种元素,所以生成物应有CO2、2SO2、2H2O.化学反应式应是:C+2H2SO4(浓)
CO2↑+2SO2↑+2H2O.
故答案为:C+2H2SO4(浓)
CO2↑+2SO2↑+2H2O;
【反思】久置的浓硫酸可能吸收了空气中的水分而变稀,所以不能反应.
故答案为:浓硫酸由于吸水浓度变稀.
 解:
解:猜想3:大家认为产生的气体可能是H2O、CO2、SO2中的两种或三种,除猜想1和猜想2外,还应有SO2和CO2.
故答案为:SO2和CO2;
【结论】浓硫酸与焦炭在加热的条件下反应,根据质量守恒定律可知,生成物质要有C、H、O、S几种元素,所以生成物应有CO2、2SO2、2H2O.化学反应式应是:C+2H2SO4(浓)
| ||
故答案为:C+2H2SO4(浓)
| ||
【反思】久置的浓硫酸可能吸收了空气中的水分而变稀,所以不能反应.
故答案为:浓硫酸由于吸水浓度变稀.
点评:此题以实验探究的形式考查学生提取有用信息的能力,并培养根据所给信息解决实际问题的能力.

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案
相关题目


