题目内容
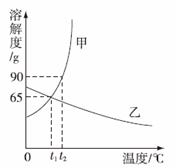
右图是甲、乙两种物质的溶解度曲线,请结合该图回答问题:
(1)  ℃时,甲、乙两种物质的溶解度相等。
℃时,甲、乙两种物质的溶解度相等。
(2)溶解度随温度升高而降低的物质是 (填“甲”或“乙”)。
(3)可使甲物质从其饱和溶液中结晶析出的方法是 。
(4)t2 ℃时,分别将甲、乙两种物质的饱和溶液降温到t1 ℃,甲溶液的溶质质量分数 (填“大于”“等于”或“小于”)乙溶液的溶
℃,甲溶液的溶质质量分数 (填“大于”“等于”或“小于”)乙溶液的溶 质质量分数。
质质量分数。
(5)小明同学用甲物质进行以下实验:
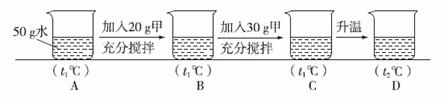
①实验过 程中,B、C、D对应的溶液为不饱和溶液的是 。
程中,B、C、D对应的溶液为不饱和溶液的是 。
②向B对应的溶液中再加入30 g甲固体的过程中,发现固体全部溶解,一段时间后又有部分固体析出。你认为“全部溶解”的原因是 。
1)t1 (2)乙 (3)降温结晶(合理均可) (4)大于 (5)①B ②甲物质溶于水时会放出热量,使溶液温度升高,甲物质的溶解度增大
解析:(1)甲、乙两物质的溶解度曲线在t1 ℃时有交点,说明甲、乙两种物质在t1 ℃时的溶解度相等。(2)乙物质的溶解度曲线随温度升高呈下降趋势,因此乙物质的溶解度是随温度的升高而降低的。(3)甲物质的溶解度曲线比较陡,说明甲物质的溶解度受温度变化影响较大,因此可以采用降温结晶的方法使甲物质从其饱和溶液中析出。(4)t1 ℃时甲、乙两物质的溶解 度均为65 g,当甲物质由t2 ℃降至t1 ℃,溶解度减小,溶液为t1 ℃时的饱和溶液,而乙物质由t2 ℃降至t1 ℃,溶解度变大,溶液为t1 ℃时的不饱和溶液,因此甲溶液的溶质质量分数大于乙溶液的溶质质量分数。(5)①t1 ℃时甲物质的溶解度为65 g,因此在50 g水中最多能溶解甲32.5 g。将20 g甲放入50 g水中所得的B溶液为不饱和溶液;再加入30 g甲充分搅拌后会有17.5 g(20 g+30 g-32.5 g)的甲没溶解,即C溶液为饱和溶液;升温至t2 ℃时甲物质的溶解度为90 g,即在50 g水中只能溶解45 g的甲物质,此时仍会有5 g(20 g+30 g-45 g)的甲没有溶解,即D溶液为饱和溶液;因此在B、C、D对应的溶液中只有B为不饱和溶液。②t1 ℃时在50 g水中最多能溶解32.5 g甲物质,而题中将50 g甲物质放入50 g水中“全部溶解”原因只能是甲物质在溶解过程中放出热量,使溶液的温度升高,而甲物质的溶解度随温度的升高而增大,从而使甲全部溶解;当一段时间后,溶液温度降到t1 ℃时仍要析出不能溶解的(50-32.5) g甲物质。
度均为65 g,当甲物质由t2 ℃降至t1 ℃,溶解度减小,溶液为t1 ℃时的饱和溶液,而乙物质由t2 ℃降至t1 ℃,溶解度变大,溶液为t1 ℃时的不饱和溶液,因此甲溶液的溶质质量分数大于乙溶液的溶质质量分数。(5)①t1 ℃时甲物质的溶解度为65 g,因此在50 g水中最多能溶解甲32.5 g。将20 g甲放入50 g水中所得的B溶液为不饱和溶液;再加入30 g甲充分搅拌后会有17.5 g(20 g+30 g-32.5 g)的甲没溶解,即C溶液为饱和溶液;升温至t2 ℃时甲物质的溶解度为90 g,即在50 g水中只能溶解45 g的甲物质,此时仍会有5 g(20 g+30 g-45 g)的甲没有溶解,即D溶液为饱和溶液;因此在B、C、D对应的溶液中只有B为不饱和溶液。②t1 ℃时在50 g水中最多能溶解32.5 g甲物质,而题中将50 g甲物质放入50 g水中“全部溶解”原因只能是甲物质在溶解过程中放出热量,使溶液的温度升高,而甲物质的溶解度随温度的升高而增大,从而使甲全部溶解;当一段时间后,溶液温度降到t1 ℃时仍要析出不能溶解的(50-32.5) g甲物质。

 名校课堂系列答案
名校课堂系列答案 14、右图是甲、乙两种物质的溶解度曲线.在t2℃时向盛有100 g水的烧杯中先后加入w g甲 和w g乙(两种物质溶解时互不影响),充分搅拌.下列说法正确的是( )
14、右图是甲、乙两种物质的溶解度曲线.在t2℃时向盛有100 g水的烧杯中先后加入w g甲 和w g乙(两种物质溶解时互不影响),充分搅拌.下列说法正确的是( ) 13、右图是甲、乙两种物质的溶解度曲线,请依据该图判断下列说法正确的是( )
13、右图是甲、乙两种物质的溶解度曲线,请依据该图判断下列说法正确的是( ) 27、右图是甲、乙两种物质的溶解度曲线,请依据该图回答下列问题:
27、右图是甲、乙两种物质的溶解度曲线,请依据该图回答下列问题: (2011?葫芦岛)右图是甲、乙两种物质的溶解度曲线,下列说法正确的是( )
(2011?葫芦岛)右图是甲、乙两种物质的溶解度曲线,下列说法正确的是( ) (2008?邵阳)右图是甲、乙两种物质的溶解度曲线,两个烧杯中各盛有20℃时上述两种物质的饱和溶液.请你通过分析,回答下列问题:
(2008?邵阳)右图是甲、乙两种物质的溶解度曲线,两个烧杯中各盛有20℃时上述两种物质的饱和溶液.请你通过分析,回答下列问题: