题目内容
1.教材的实践活动中提到用碱溶液可以制作“叶脉书签”,“我爱生活,我爱化学”学习小组用20g含碳酸钠53%的天然碱制取氢氧化钠用于制作“叶脉书签”(杂质不参加反应).操作过程如下: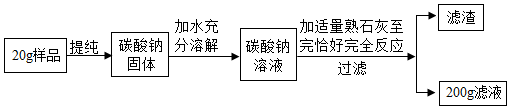
请计算:
(1)20g样品中碳酸钠的质量为10.6 g
(2)反应后所得滤液中氢氧化钠的质量分数为多少?(写出计算过程)
(3)将200g滤液浓缩制成“叶脉书签”所需质量分数为10%的氢氧化钠溶液,需蒸发水120 g.
分析 (1)碳酸钠的质量=样品的质量×含碳酸钠的质量分数;
(2)根据化学方程式结合碳酸钠的质量求解氢氧化钠的质量,进一步计算所得滤液中氢氧化钠的质量分数;
(3)根据溶液稀释前后溶质质量不变解答.
解答 解:(1)碳酸钠的质量为20g×53%=10.6g;
(2)设反应生成氢氧化钠的质量为x;
Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
106 80
10.6g x
$\frac{106}{10.6g}=\frac{80}{x}$
解得x=8g
氢氧化钠的质量分数=$\frac{8g}{200g}$×100%=4%
答:反应后所得滤液中氢氧化钠的质量分数为4%.
(3)设需蒸发水y
200g×4%=(200g-y)×10%
y=120g
故答案为:
(1)10.6;(2)4%;(3)120.
点评 本题重点考查了化学方程式的有关计算方法、步骤和格式;它是一道很传统的根据化学方程式计算的题目.解答时,只要细心地分析审题后,按照有关化学方程式的计算步骤和格式,进行计算即可.

练习册系列答案
相关题目
12.下列归纳全部正确的是( )
| A、实验记录 | B、生活化学 |
| ①用量筒量取7.25毫升水 ②用托盘天平称取9.76g的NaCl固体 | ①将硝酸铵溶于水制作“冷敷包” ②人体缺锌易导致侏儒症 |
| C、解释说明 | D、化学原理 |
| ①稀有气体作保护气,因为其化学性质稳定 ②波尔多液不能用铁桶盛放,因为其含有CuSO4 | ①酸雨形成的原因 CO2+H2O=H2CO3 ②铝制品耐腐的原因 4Al+3O2=2Al2O3 |
| A. | A | B. | B | C. | C | D. | D |

 利用如图所示装置探究燃烧的条件(试管中是空气).
利用如图所示装置探究燃烧的条件(试管中是空气).