题目内容
17.下列有关叙述正确的是( )| A. | 碱溶液有许多共同性质,是因为它们的溶液中都含OH- | |
| B. | 应加大力度大量开采化石燃料,以满足社会发展的需求 | |
| C. | 灭火的根本就是要改变可燃物的着火点 | |
| D. | 家用天然气、煤气或液化气发生泄漏时,应立即开灯检查 |
分析 A、根据碱具有相似化学性质的原因,进行分析判断.
B、根据化石燃料属于不可再生资源,进行分析判断.
C、根据灭火的原理,进行分析判断.
D、根据可燃性气体与空气混合后遇明火或遇电火花等可能发生爆炸,进行分析判断.
解答 解:A、物质的结构决定物质的性质,碱溶液有许多共同性质,是因为它们的溶液中都含OH-,故选项说法正确.
B、化石燃料属于不可再生资源,大量开采化石燃料会大大缩短化石燃料的使用年限,会引发一系列问题,故选项说法错误.
C、可燃物的着火点一般是不变的,不能改变可燃物的着火点,故选项说法错误.
D、家用天然气、煤气或液化气发生泄漏时,立即开灯检查会产生电火花,可能发生爆炸,故选项说法错误.
故选:A.
点评 本题难度不大,掌握碱的化学性质、灭火的原理、防止爆炸的措施等是正确解答本题的关键.

练习册系列答案
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案
相关题目
2.除杂设计(括号内为杂质)所选试剂和操作都正确的是( )
| 序号 | 物质 | 选用试剂 | 操作 |
| A | CO2 (HCl) | NaOH溶液 | 洗气 |
| B | KC1O3 固体(KC1) | 加热至不再产生气体 | |
| C | KNO3 溶液(KOH) | CuSO4溶液 | 加入适量试剂,过滤、蒸发 |
| D | MgCl2 溶液(NaCl) | ①KOH溶液 ②稀盐酸 | 加入过量试剂①,过滤、洗涤 向所得固体中加入适量试剂②至固体恰好溶解 |
| A. | A | B. | B | C. | C | D. | D |
3. 化学兴趣小组同学发现实验台上有两瓶标签破损的试剂瓶.小组同学针对这两瓶试剂展开研究:
化学兴趣小组同学发现实验台上有两瓶标签破损的试剂瓶.小组同学针对这两瓶试剂展开研究:
【提出问题】这两瓶试剂分别是什么?
【查阅资料】
①碱性的亚硫酸钠(Na2SO3)溶液、Na2CO3溶液都能与中性的CaCl2溶液发生复分解反应,产生白色沉淀.
②Na2SO3+2HCl═2NaCl+SO2↑+H2O.
【作出猜想】溶液可能分别是NaOH、Na2CO3、Na2SO3或NaCl溶液中的一种.
【限选试剂】酚酞试液、稀盐酸、石灰水、氯化钙溶液
【实施方案】
【实验反思】同学们经过分析,认为A溶液还可能是变质的NaOH溶液,请你利用上述试剂设计鉴定实验方案,完成实验报告.
 化学兴趣小组同学发现实验台上有两瓶标签破损的试剂瓶.小组同学针对这两瓶试剂展开研究:
化学兴趣小组同学发现实验台上有两瓶标签破损的试剂瓶.小组同学针对这两瓶试剂展开研究:【提出问题】这两瓶试剂分别是什么?
【查阅资料】
①碱性的亚硫酸钠(Na2SO3)溶液、Na2CO3溶液都能与中性的CaCl2溶液发生复分解反应,产生白色沉淀.
②Na2SO3+2HCl═2NaCl+SO2↑+H2O.
【作出猜想】溶液可能分别是NaOH、Na2CO3、Na2SO3或NaCl溶液中的一种.
【限选试剂】酚酞试液、稀盐酸、石灰水、氯化钙溶液
【实施方案】
| 实验 | 实验操作 | 实验现象 | 实验结论 |
| 实验一 | 分别取少量待测液于试管中,向其中滴入酚酞试液 | 溶液变成红色 | 不可能是氯化钠溶液 |
| 实验二 | 另取少量待测液于试管中,向其中各滴入澄清石灰水 | 产生白色沉淀 | 可能是Na2SO3溶液和Na2CO3溶液中的一种,写出其中一个反应的化学方程式Na2CO3+Ca(OH)2=CaCO3↓+2NaOH 或Na2SO3+Ca(OH)2=CaSO3↓+2NaOH |
| 实验三 | 另取少量待测液于试管中,分别加入足量的稀盐酸. | 若有无色无味的气体产生 | A是Na2CO3溶液 |
| 若有刺激性气味的气体产生 | B是Na2SO3溶液 |
| 实验操作 | 实验现象 | 实验结论 |
| 取少量A溶液于试管中,加入足量CaCl2溶液,再向上层清液中滴加无色酚酞溶液 | 产生白色沉淀,且溶液变成红色 | A溶液是部分变质的NaOH溶液 |
4.在高速发展的信息时代,我们要学会获取和辨别信息.下列信息中正确的是( )
| A. | 为了提高粮食产量,应大量使用农药、化肥 | |
| B. | 为保鲜海鲜产品,应用甲醛浸泡 | |
| C. | 碘元素有“聪明元素”的美称,炒菜时应加入大量的加碘盐 | |
| D. | 为使木材燃烧有充足的氧气,应将木柴架空 |
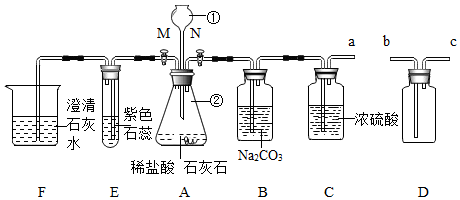
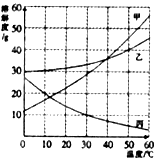 化学是与我们的生产和生活紧密相关的学科
化学是与我们的生产和生活紧密相关的学科