题目内容
12.根据物质的组成和结构,分析下列各组物质中性质不同的原因.(1)金刚石和石墨碳原子的排列不同.
(2)一氧化碳和二氧化碳分子的构成不同.
(3)Mg2+与Mg的性质不同核外电子数及微粒结构不同.
分析 (1)金刚石和石墨是碳元素的两种单质,它们互为同素异形体,但是由于它们碳原子的排列方式不同,所以虽然它们化学性质基本相同物理性质却有很大差异;
(2)一个CO分子中只有1个氧原子,具有较强还原性.②CO2中的碳已是最高价,不具有还原性.
(3)根据Mg2+与Mg的微粒结构进行分析;
解答 解:(1)金刚石和石墨性质不同的原因为碳原子的排列不同;
(2)一氧化碳和二氧化碳性质不同的原因为分子的构成不同,一个CO中只有1个氧原子,还能获得一个氧原子;CO2不能再获得氧原子,不具有还原性;
(3)Mg2+与Mg的核外电子数及微粒结构不同,Mg2+的核外有10个电子,最外层8个,达到了稳定结构;Mg的核外有12个电子,最外层2个电子,化学性质活泼;
故答案为:(1)碳原子的排列不同;(2)分子的构成不同;(3)核外电子数及微粒结构不同;
点评 物质的组成与结构决定物质的性质,而物质的性质又决定着物质的用途,所以要想了解某种物质的用途,还得从根本上了解物质的结构.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
2.打开装有下列试剂的试剂瓶盖后,在瓶口出现白雾的是( )
| A. | 浓硫酸 | B. | 浓盐酸 | C. | 氢氧化钠固体 | D. | 澄清石灰水 |
3.第112号化学元素符号为“Cn”.其相对原子质量为277,是目前获得正式承认的最重的元素,则该元素原子核内的中子数为( )
| A. | 112 | B. | 277 | C. | 165 | D. | 389 |
17.下列各图所示初中化学常见的实验操作中,正确的是( )
| A. | 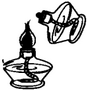 点燃酒精灯 | B. | 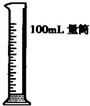 量9.5mL液体 | C. | 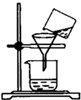 过滤 | D. | 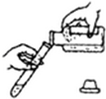 倾倒液体 |
1.空气质量日报中不需报告的是( )
| A. | 二氧化硫 | B. | 一氧化碳 | C. | 可吸入颗粒物 | D. | 二氧化碳 |