题目内容
【题目】A~J为初中常见的物质,它们可以发生如图所示的关系。其中A是常用的溶剂,C和D是组成元素相同的气体,E是一种显碱性的钠盐,俗称为苏打,F是一种常见的强碱溶液,G是一种蓝色沉淀,H可用来配制农药波尔多液,J为黑色固体。回答下列问题:
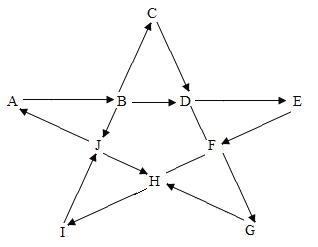
(1)写出物质B、I的化学式____________________ 、_____________ 。
(2)写出反应E→F的化学方程式__________________________________。
(3)反应H→I为_____________________________反应(填基本反应类型);
(4)写出物质C的一种用途_____________________________。
【答案】O2 Cu ![]() 置换 作燃料( 或冶炼金属)
置换 作燃料( 或冶炼金属)
【解析】
A是常用的溶剂,最常见的是H2O, C和D是组成元素相同的气体,则C、D分别为CO和CO2中的一种,E是显碱性的钠盐,俗称为苏打,则E为Na2CO3,D能生成E,故D为CO2,C为CO,H2O能生成B,且B能生成一氧化碳和二氧化碳,可推出B是O2,F是一种常见的强碱溶液,则F为NaOH,G是一种蓝色沉淀,可推出G为Cu(OH)2,H可用来配制农药波尔多液,且H与F能发生反应,故H为CuSO4,H能生成I,则I中含有铜元素或硫酸根离子,且I能生成黑色固体J,则推断出J为黑色的CuO,故I为Cu。
(1)物质B为氧气,化学式为O2,物质I为铜,化学式为Cu;
(2)E为碳酸钠,F为氢氧化钠,碳酸钠可与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,其化学反应方程式为:![]() ;
;
(3)H为硫酸铜,I为铜,铁可与硫酸铜溶液反应生成硫酸亚铁和铜,其化学反应方程式为:![]() ,该反应符合一种单质与一种化合物反应生成另一种单质与另一种化合物的反应,属于置换反应;
,该反应符合一种单质与一种化合物反应生成另一种单质与另一种化合物的反应,属于置换反应;
(4)C为一氧化碳,CO可用来作燃料或冶炼金属。

【题目】小雨阅读课外资料得知:过氧化氢分解除了用二氧化锰还可用氧化铜等物质作催化剂,于是她对氧化铜产生了探究兴趣。
(提出问题)氧化铜是否也能作氯酸钾分解的催化剂?它是否比二氧化锰催化效果更好?
(设计实验)小雨以生成等体积的氧气为标准,设计了下列三组实验(其他可能影响实验的因素均忽略)。
实验序号 | 氯酸钾质量 | 其他物质质量 | 待测数据 |
① | 1.2g | — | |
② | 1.2g | 氧化铜0.5g | |
③ | 1.2g | 二氧化锰0.5g |
(1)上述实验应测量的“待测数据”是_____。
(2)若实验②比实验①的“待测数据”更_____(填“大”或“小”),说明氧化铜能加快氯酸钾的分解速率。
(3)将实验②反应后的固体加水溶解、过滤、洗涤、干燥,若称量得到![]() 黑色粉末,说明_____。
黑色粉末,说明_____。
(4)再将黑色粉末放入试管中,加入_____,若观察到_____,说明黑色粉末的化学性质在反应前后保持不变。
(预期结论)氧化铜也能作氯酸钾分解的催化剂。
(评价设计)你认为小雨设计实验③和实验②对比的目的是_____。