题目内容
65g 锌可以跟300g 硫酸溶液恰好完全反应.计算:
①可制得氢气多少克?
②这种硫酸溶液中溶质的质量分数是多少?
③100g 这种硫酸稀释成10% 的硫酸,需加水多少克?
①可制得氢气多少克?
②这种硫酸溶液中溶质的质量分数是多少?
③100g 这种硫酸稀释成10% 的硫酸,需加水多少克?
考点:根据化学反应方程式的计算,用水稀释改变浓度的方法,有关溶质质量分数的简单计算
专题:溶质质量分数与化学方程式相结合的计算
分析:①锌与硫酸恰好完全反应,根据反应的化学方程式,由金属锌的质量计算生成氢气的质
量、硫酸溶液中溶质的质量;
②根据上述计算,利用溶质质量分数公式计算稀硫酸溶液的质量分数;
③根据加水稀释,稀释前后溶质质量不变;
量、硫酸溶液中溶质的质量;
②根据上述计算,利用溶质质量分数公式计算稀硫酸溶液的质量分数;
③根据加水稀释,稀释前后溶质质量不变;
解答:解:①设反应放出氢气质量为x,消耗硫酸溶液中溶质的质量为y.
Zn+H2SO4=ZnSO4+H2↑
65 98 2
65g y x
=
,
=
x=2g,y=98g;
②这种硫酸溶液中溶质的质量分数是:
×100%=32.7%;
③100g 这种硫酸稀释成10% 的硫酸,需加水的质量为W
100g×32.7%=(100+w)×10% 解得:w=227g;
答:①可制得氢气是2克;②这种硫酸溶液中溶质的质量分数是32.7%;③100g 这种硫酸稀释成10% 的硫酸,需加水227克.
Zn+H2SO4=ZnSO4+H2↑
65 98 2
65g y x
| 65 |
| 65g |
| 2 |
| x |
| 65 |
| 65g |
| 98 |
| y |
x=2g,y=98g;
②这种硫酸溶液中溶质的质量分数是:
| 98g |
| 300g |
③100g 这种硫酸稀释成10% 的硫酸,需加水的质量为W
100g×32.7%=(100+w)×10% 解得:w=227g;
答:①可制得氢气是2克;②这种硫酸溶液中溶质的质量分数是32.7%;③100g 这种硫酸稀释成10% 的硫酸,需加水227克.
点评:本题主要考查了根据化学方程式的计算、有关溶液的计算.浓溶液加水稀释,溶液溶质质量分数减小,但溶液中溶质的质量不变.

练习册系列答案
 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案
相关题目
制作松花皮蛋的配料有:纯碱、食盐、生石灰、草木灰(内含碳酸钾)、开水、以及米糠、稻壳等辅料.配料之间首先是生石灰与水反应生成熟石灰,试推断另外最有可能发生的化学反应是( )
| A、化合反应 | B、分解反应 |
| C、置换反应 | D、复分解反应 |

 在一烧杯中盛有50g NaOH溶液,向其中逐渐滴加溶质质量分数为10%的稀盐酸.反应生成氯化钠的总质量与所滴入稀盐酸的质量关系曲线如图所示,请根据题意回答问题:
在一烧杯中盛有50g NaOH溶液,向其中逐渐滴加溶质质量分数为10%的稀盐酸.反应生成氯化钠的总质量与所滴入稀盐酸的质量关系曲线如图所示,请根据题意回答问题: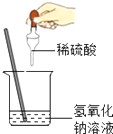 如图所示,某同学在进行酸碱中和反应的实验时,向烧杯中的氢氧化钠溶液滴加稀硫酸一会儿后,突然却发现忘记了滴加指示剂.
如图所示,某同学在进行酸碱中和反应的实验时,向烧杯中的氢氧化钠溶液滴加稀硫酸一会儿后,突然却发现忘记了滴加指示剂.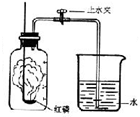 我们已经知道空气的主要成分是氮气和氧气,图为测定空气中氧气含量的实验装置示意图.
我们已经知道空气的主要成分是氮气和氧气,图为测定空气中氧气含量的实验装置示意图.