题目内容
18.向AgNO3、Cu(NO3)2、Mg(NO3)2的混合溶液中加入一定量的锌粉,充分反应后过滤,向滤液中滴加稀盐酸无白色沉淀产生.则所得滤渣中一定含有银;(填物质名称),滤液中一定含有的金属阳离子是Mg2+、Zn2+.(填离子符号)分析 在金属活动性顺序中,氢前的金属能与酸反应生成氢气,位置在前的金属能将位于其后的金属从其盐溶液中置换出来,利用此知识分析即可.
解答 解:根据在金属活动性顺序中,镁>锌>氢>铜>银,故锌不能与Mg( NO3)2溶液反应,而锌能与硝酸银反应生成银和硝酸锌,可以和硝酸铜反应生成铜和硝酸锌;根据“充分反应后过滤,向滤渣中加入稀盐酸无明显现象”,所以说明锌完全反应,而无法确定AgNO3、Cu( NO3)2中金属离子是否全置换出,但滤渣中一定会有银;所以溶液中的金属阳离子会有锌离子和没有反应的镁离子.
故答案为:
银,Mg2+、Zn2+
点评 此题考查了金属活动顺序表中锌、铜、银的金属活动性强弱,及其金属活动性顺序表的应用,锻炼了学生分析问题解决问题的能力.

练习册系列答案
 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案
相关题目
9.下列物质与稀盐酸反应不能一步实现的是( )
| A. | NaOH→H2O | B. | CuO→CuCl2 | C. | Fe→FeCl3 | D. | AgNO3→AgCl |
6.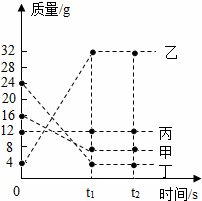 在一密闭容器中加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,测得反应前及t1、t2时各物质质量如图所示,下列说法中不正确的是( )
在一密闭容器中加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,测得反应前及t1、t2时各物质质量如图所示,下列说法中不正确的是( )
 在一密闭容器中加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,测得反应前及t1、t2时各物质质量如图所示,下列说法中不正确的是( )
在一密闭容器中加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,测得反应前及t1、t2时各物质质量如图所示,下列说法中不正确的是( )| A. | 该反应中,甲、乙的质量变化之比为1:4 | |
| B. | 丙可能为该反应的催化剂 | |
| C. | 该反应中,乙、丁的质量变化之比为7:5 | |
| D. | 该反应为化合反应 |
13.分类是学习化学的方法之一,下列各组物质是按单质、氧化物、混合物进行分类的是( )
| A. | 液氧、水、矿泉水 | B. | 活性炭、火碱、碘盐 | ||
| C. | 生铁、干冰、煤 | D. | 金刚石、熟石灰、空气 |
10.生活中的下列做法利用了物质的化学性质的是( )
| A. | 用细沙子和棉花来净化自来水 | |
| B. | 铅笔芯粉末灌入不易打开的门锁 | |
| C. | 农村用沼气作燃料烧水煮饭 | |
| D. | 在房间内放入活性炭吸收甲醛等有害气体 |
7.下列关于氧气的用途的叙述错误的是( )
| A. | 用于提高钢铁的产量和质量 | B. | 氧炔焰用来焊接或切割金属 | ||
| C. | 液氧制成炸药,用来开山采矿 | D. | 液氧可用作宇宙火箭的燃料 |
17.“洋河美酒飘香”,当走近洋河酒厂时就能闻到特殊的香味,这表明( )
| A. | 分子间有间隔 | |
| B. | 分子是保持物质化学性质的最小粒子 | |
| C. | 分子在不停地运动着 | |
| D. | 同种物质的性质相同 |