题目内容
8.为检验一瓶氢氧化钠溶液是否变质,同学们展开探究:(1)甲同学用酚酞试液检验氢氧化钠溶液是否变质,你认为它不能(填”能”或”不能”)成功,理由是碳酸钠溶液显碱性,也能使酚酞试液变红
(2)乙同学在三支试管中各放入少量的该瓶溶液,用酸、碱、盐三种物质分别检验氢氧化钠是否变质,均获得成功,她所用的试剂依次是{写化学式}:酸HCl;碱Ca(OH)2;盐CaCl2.
分析 根据氢氧化钠变质后生成的碳酸钠显碱性,也能使酚酞试液变红;检验氢氧化钠是否变质,主要验证是否存在碳酸根离子即可,加入试剂与碳酸根离子结合现象明显即可.
解答 解:(1)氢氧化钠变质后生成的碳酸钠溶液显碱性,也能使酚酞试液变红,所以用酚酞检验氢氧化钠溶液是否变质不能成功;
(2)检验氢氧化钠是否变质,主要验证是否存在碳酸根离子即可,加入试剂与碳酸根离子结合现象明显即可,所以加入稀盐酸,有气泡产生,说明已经变质,否则没变质;加入氢氧化钙,如果有白色沉淀生成,说明已经变质,否则不变质;加入氯化钙,如果有白色沉淀生成,说明已经变质,否则不变质.
故答案为:(1)不能;碳酸钠溶液显碱性,也能使酚酞试液变红;(2)HCl;Ca(OH)2;CaCl2.
点评 熟练掌握氢氧化钠和碳酸钠的性质,并知道在检验氢氧化钠是否完全变质时必须先把碳酸钠变成沉淀并且不生成影响氢氧化钠检验的碱性物质,才能使用酚酞检验氢氧化钠.

练习册系列答案
相关题目
19.清凉油具有散热、醒脑、提神的功效,其主要成分为薄荷脑(化学式为C10H20O),下列有关薄荷脑的说法正确的是( )
| A. | 薄荷脑中碳元素的质量分数很大 | B. | 薄荷脑中含有10个碳原子 | ||
| C. | 薄荷脑的相对分子质量是156g | D. | 薄荷脑中碳、氢元素的质量比为1:2 |
3.下列说法正确的是( )
| A. | 盐都能食用,故称为食盐 | B. | 盐就是食盐,易溶于水 | ||
| C. | 盐都有咸味,都是白色固体 | D. | 盐是一类物质的总称 |
13.甲同学家新换了水龙头,从说明书上了解到该水龙头是铜质镀铬的.她想到在学过的金属活动性顺序中并没有金属铬,为比较铬与常见金属铁、铜的活动性强弱,她和同学们在应用所学知识进行分析的基础上,提出了以下猜想,并进行了实验探究.
【作出猜想】
猜想1.Cr>Fe>Cu; 猜想2.Fe>Cu>Cr; 猜想3.你的猜想是Fe>Cr>Cu.
【查阅资料】
①铬(Cr)是银白色有光泽的金属,在空气中其表面能生成抗腐蚀的致密的氧化膜.
②铬能与稀硫酸反应,生成蓝色的硫酸亚铬(CrSO4)溶液.
【实验药品】
铁片、铬片、铜片、稀硫酸、CuSO4溶液、CrSO4溶液、FeSO4溶液.(溶液均为新制)
【甲同学实验】
甲同学取大小相等的三种金属片,用砂纸打磨光亮;再取三支试管,分别放入等量的稀硫酸.
【乙同学实验】
乙同学为验证甲同学的结论,又设计了以下实验.
【实验反思】
(1)你认为乙同学没有必要做的实验是试管5中的实验没有必要做.
(2)请你结合所给的实验药品再设计一个实验,验证甲同学的结论.
【作出猜想】
猜想1.Cr>Fe>Cu; 猜想2.Fe>Cu>Cr; 猜想3.你的猜想是Fe>Cr>Cu.
【查阅资料】
①铬(Cr)是银白色有光泽的金属,在空气中其表面能生成抗腐蚀的致密的氧化膜.
②铬能与稀硫酸反应,生成蓝色的硫酸亚铬(CrSO4)溶液.
【实验药品】
铁片、铬片、铜片、稀硫酸、CuSO4溶液、CrSO4溶液、FeSO4溶液.(溶液均为新制)
【甲同学实验】
甲同学取大小相等的三种金属片,用砂纸打磨光亮;再取三支试管,分别放入等量的稀硫酸.
| 实验 | 实验操作 | 实验现象 | 结论与解释 |
| 试管1 | 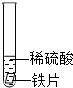 | 铁片表面产生气泡较慢,溶液变为浅绿色. | (1)实验前用砂纸打磨金属片的目的是 除去金属表面的氧化膜. (2)甲同学得到的结论是猜想1正确,他得到此结论的依据是 试管1中实验现象铁片表面产生气泡较慢,溶液变为浅绿色,可知金属铁在金属活动顺序中排在氢前,根据铬片表面产生气泡较快,溶液变为蓝色,从而得出铬也排在氢前且铬比铁活泼,因为铜不能和稀硫酸反应生成氢气. |
| 试管2 | 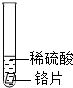 | 铬片表面产生气泡较快,溶液变为蓝色. | |
| 试管3 | 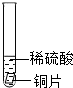 | 铜片上没有变化. |
乙同学为验证甲同学的结论,又设计了以下实验.
| 实验 | 实验操作 | 实验现象 | 结论与解释 |
| 试管4 | 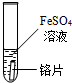 | \ | (1)甲同学的结论正确. (2)请写出铬与硫酸铜反应的化学方程式 Cr+CuSO4=CuSO4+Cr. |
| 试管5 | 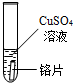 |
(1)你认为乙同学没有必要做的实验是试管5中的实验没有必要做.
(2)请你结合所给的实验药品再设计一个实验,验证甲同学的结论.
| 实验操作 | 实验现象 | 结论与解释 |
在试管中放入打磨光亮的铁片,再加入CrSO4溶液 | 铁片没有变化 | 甲同学的结论正确. |