题目内容
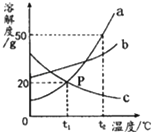
【题目】20℃时,根据某固体物质在不同质量的水中达到饱和状态时所溶解的质量,绘制成如图所示的斜线,回答下列问题:
(1)20℃时,该固体物质的溶解度为 .
(2)C点所对应的溶液是(填“饱和溶液”或“不饱和溶液”).
(3)若从D点溶液得到A点溶液,需增加该溶质g.
(4)图中四点所对应的溶液质量分数大小关系为 .
【答案】
(1)88g
(2)不饱和
(3)44
(4)A=B>C>D
【解析】解:(1)20℃时,100g水中最多溶解的质量为88g,故20℃时该物质的溶解度为88g,故填:88g;(2)在曲线上的点和曲线上边的点都是饱和状态,在曲线下边的点属于不饱和状态,所以C点对应的溶液是不饱和状态,故填:不饱和;(3)从D点溶液得到A点溶液,需增加该溶质:88g﹣44g=44g,故填:44;(4)点A和点B都在线上,点C和点D含有的溶质相同,C点对应的溶液中溶剂少,故溶质质量分数大于D点,故四点所对应的溶液质量分数大小关系为A=B>C>D,故填:A=B>C>D.
【考点精析】掌握饱和溶液和不饱和溶液和固体溶解度的概念是解答本题的根本,需要知道饱和与不饱和的判断方法:看有无不溶物或继续加入该溶质,看能否溶解;溶解度定义:在一定温度下,某固态物质在100g溶剂里达到饱和状态时所溶解的质量;四要素:①条件:一定温度②标准:100g溶剂③状态:达到饱和④质量:单位:克.

【题目】某化学兴趣小组为了测定某石灰石样品中碳酸钙的质量分数,取用15g石灰石样品,把50g稀盐酸分五次加入样品中(样品中的杂质既不与盐酸反应,也不溶解于水),每次充分反应后都经过滤、干燥、称量,得实验数据如下:
实验次数 | 1 | 2 | 3 | 4 | 5 |
稀盐酸的累计加入量 | 10g | 20g | 30g | 40g | 50g |
剩余固体的质量 | 12g | 9g | 6g | 5g | 5g |
请计算:
(1)石灰石中碳酸钙的质量分数为多少?
(2)最终生成二氧化碳的质量是多少?