题目内容
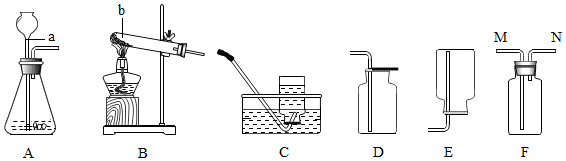
12. 实验室有一瓶保管不当的试剂(如图),其残缺的标签中只剩下“Na”和“10%”字样.已知它是无色液体,是初中化学常用的试剂.小强和小华同学很感兴趣,决定对其成分进行探究:
实验室有一瓶保管不当的试剂(如图),其残缺的标签中只剩下“Na”和“10%”字样.已知它是无色液体,是初中化学常用的试剂.小强和小华同学很感兴趣,决定对其成分进行探究:【提出问题】这瓶试剂可能是什么溶液呢?
【交流讨论】根据受损标签的情况判断,这瓶试剂不可能是A.
A.酸 B.碱 C盐
【查阅资料】
I.初中化学常见的含钠化合物有NaCl、NaOH、Na2CO3、NaHCO3.
Ⅱ.Na2CO3和NaHCO3溶液都呈碱性.
Ⅲ.测定室温(20℃)时,四种物质的溶解度的数据如下:
| 物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
| 溶解度/g | 36 | 109 | 215 | 9.6 |
【作出猜想】①可能是NaOH溶液;②可能是Na2CO3溶液;③可能是NaCl.
【设计并实验】
(1)小强用洁净的玻璃棒蘸取该溶液滴在pH试纸上,测得pH>7.这瓶试剂不可能是NaCl.
(2)小强为了检验该溶液是NaOH溶液还是Na2C03溶液,他又进行了如下实验:
| 操作步骤 | 实验现象 | 结论及化学方程式 |
| 取样于试管中,滴加 氢氧化钙溶液 | 有白色沉淀生成 | 猜想②正确. 相关的化学方程式Na2CO3+Ca(OH)2═CaCO3↓+2NaOH |
分析 【交流讨论】从酸是由氢离子和酸根离子构成的,所以酸的化学式最左边应为氢元素(H)去分析解答;
【作出猜想】由【查阅资料】Ⅰ、初中化学常见的含钠化合物有NaCl、NaOH、Na2CO3去分析解答;
【设计并实验】
(1)由于氢氧化钠是碱,所以其溶液显碱性,由【查阅资料】可知:碳酸钠溶液显碱性;NaCl是中性的去分析解答;
(2)从表中结论:“猜想②正确”说明瓶中溶液为碳酸钠溶液去分析解答;
解答 解:【交流讨论】由于酸是由氢离子和酸根离子构成的,所以酸的化学式最左边应为氢元素(H),而标签中最左边的元素是Na元素;故答案为:A;
【得出结论】根据常温下碳酸氢钠的溶液为9.6g,可判断常温下碳酸氢钠的饱和溶液的溶质质量分数=$\frac{9.6g}{100g+9.6g}$×100%=8.8%,因此可判断该溶液不可能为碳酸氢钠溶液;故答案为:NaHCO3
【作出猜想】除碳酸氢钠外,该溶液可能为氯化钠、碳酸钠或氢氧化钠溶液;故答案为:NaOH
【设计并实验】
(1)由于氢氧化钠是碱,所以其溶液显碱性,由【查阅资料】可知:碳酸钠溶液显碱性;NaCl是中性的;小强用洁净的玻璃棒蘸取该溶液滴在pH试纸上,测得pH>7,说明该溶液显碱性,故不可能是NaCl;故答案为:NaCl;
(2)取样于试管中,滴加氢氧化钙溶液,碳酸钠溶液和氢氧化钙溶液反应生成不溶于水的碳酸钙(白色)和氢氧化钠,其反应的化学方程式为:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH;由氢氧化钙和氢氧化钠都属于碱,二者不会发生反应;由于表中结论:“猜想②正确”说明瓶中溶液为碳酸钠溶液;故答案为:有白色沉淀生成;Na2CO3+Ca(OH)2═CaCO3↓+2NaOH;
点评 本题综合利用了物质的组成、物质的溶解性、溶液的酸碱性及物质的变化规律对未知物质进行鉴别,体现运用化学知识分析问题、解决问题的能力.

| A. | 海水晒盐 | B. | 蜡烛燃烧 | C. | 煤的干馏 | D. | 粉尘爆炸 |
| 物 质 | 杂 质 | 除杂试剂 | 提 纯 方 法 | |
| A | CO2 | CO | O2 | 点燃 |
| B | KCl | MnO2 | 水 | 溶解、过滤、蒸发 |
| C | CaO | CaCO3 | 稀盐酸 | 溶解、过滤 |
| D | KNO3 | NaCl | H2O | 溶解、蒸发、过滤 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 金Au>银Ag>铜Cu | B. | 钾K>钙Ca>钠Na | C. | 锡Sn>铁Fe>贡Hg | D. | 铁Fe>镁Mg>铜Cu |
| A. | 蜡烛燃烧产生明亮的火馅 | |
| B. | 蜡烛燃烧时有少量白烟在火馅上方 | |
| C. | 吹灭蜡烛后,有白烟,白烟能被点着,蜡烛会复燃 | |
| D. | 火焰上方罩干冷的烧杯,烧杯内壁有水雾且温度升高 |