题目内容
20.我们学完“物质构成的奥秘”,认识了微观世界和宏观现象.根据图示填空: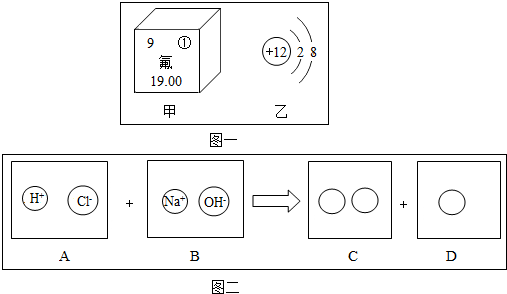
(1)图一甲中,①代表的元素符号是F,其原子的结构示意图为
 ,则由甲、乙元素组成化合物氟化镁的化学式为MgF2;
,则由甲、乙元素组成化合物氟化镁的化学式为MgF2;(2)图二体现了稀盐酸和氢氧化钠溶液反应的实质,图中C、D中圆圈内应填入的化学式或离子符号是:CNa+和Cl-,DH2O;
(3)用化学方程式表示B物质与硫酸铜溶液的反应2NaOH+CuSO4=Na2SO4+Cu(OH)2↓;其反应类型是复分解反应.
分析 (1)根据元素的原子序数确定元素写出符号,根据元素的化合价写出形成化合物的化学式;
(2)根据中和反应的实质分析图中C、D中圆圈内应填入的化学式或离子符号;
(3)根据氢氧化钠与与硫酸铜溶液的反应写出反应的化学方程,根据反应的特点分析反应的类型.
解答 解:(1)由图一甲中原子的序数是9可知,①代表的元素氟元素,符号是F,其原子的最外层有7个电子,易得到一个电子,在化合物中显-1价,乙元素的质子数是12,属于镁元素,化合价为+2价,组成化合物氟化镁的化学式为:MgF2;
(2)图二体现了稀盐酸和氢氧化钠溶液反应的实质,中和反应的实质是氢离子与氢氧化根离子结合生成了水,图中C、D中圆圈内应填入的化学式或离子符号是:C Na+和Cl-,D H2O;
(3)由图示可知,B物质是氢氧化钠,与硫酸铜溶液的反应的方程式是:2NaOH+CuSO4=Na2SO4+Cu(OH)2↓;其反应类型是复分解反应.
故答为:(1)F,MgF2;(2)Na+和Cl-,H2O;(3)2NaOH+CuSO4=Na2SO4+Cu(OH)2↓,复分解反应.
点评 本题主要考查了原子结构示意图的意义,最外层电子数的多少和原子得失电子的关系,中和反应的实质等知识,培养学生应用知识解决问题的能力.

练习册系列答案
相关题目
10.某些化合物在形成时,不同元素的原子各自提供电子,形成共用电子对.在这种情况下,元素化合价的数值就是形成共用电子对的数目.在一个H2S分子中,硫原子形成的共用电子对数目为( )
| A. | 1个 | B. | 2个 | C. | 3个 | D. | 4个 |
11. 铬是人体必需的一种微量元素,但铬过量摄入对人体危害非常大,铬的毒性与其存在形式有关.河北、浙江等多地不法厂家生产的“毒胶囊”中主要含有毒性最大的+6价铬元素,如图为有关铬元素的信息,下列说法错误的是( )
铬是人体必需的一种微量元素,但铬过量摄入对人体危害非常大,铬的毒性与其存在形式有关.河北、浙江等多地不法厂家生产的“毒胶囊”中主要含有毒性最大的+6价铬元素,如图为有关铬元素的信息,下列说法错误的是( )
 铬是人体必需的一种微量元素,但铬过量摄入对人体危害非常大,铬的毒性与其存在形式有关.河北、浙江等多地不法厂家生产的“毒胶囊”中主要含有毒性最大的+6价铬元素,如图为有关铬元素的信息,下列说法错误的是( )
铬是人体必需的一种微量元素,但铬过量摄入对人体危害非常大,铬的毒性与其存在形式有关.河北、浙江等多地不法厂家生产的“毒胶囊”中主要含有毒性最大的+6价铬元素,如图为有关铬元素的信息,下列说法错误的是( )| A. | 毒胶囊中化学成分可能是K2CrO4 | B. | 铬元素属于非金属元素 | ||
| C. | 铬元素的相对原子质量为52.00 | D. | 铬的硬度和抗腐蚀性能都很强 |
8.分类是化学学习过程中常用的方法,下列分类中正确的是( )
| A. | 合成材料:涤纶、塑料、玻璃 | |
| B. | 氧化物:生石灰、铁锈、二氧化锰 | |
| C. | 合金:生铁、锰钢、青铜 | |
| D. | 复合肥料:磷酸二氢钙、尿素、硝酸钾 |
15.下列实验操作错误的是( )
| A. | 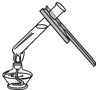 给液体加热 | B. | 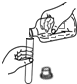 倾倒液体 | C. | 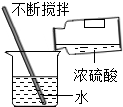 稀释浓硫酸 稀释浓硫酸 | D. | 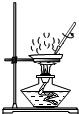 蒸发食盐水 |
12.20℃时,KNO3的溶解度为31.6g.此温度下,在100g水中形成的KNO3溶液的叙述中,不正确的是( )
| A. | 饱和溶液的容剂质量是100g | B. | 不饱和溶液的容剂质量是100g | ||
| C. | 饱和溶液的容剂质量是31.6g | D. | 不饱和溶液的容剂质量是31.6g |
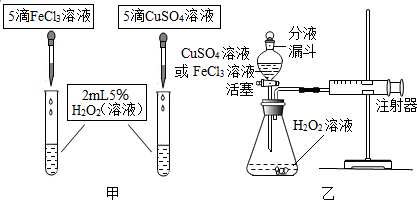
9.为比较相同浓度的FeCl3溶液和CuSO4溶液对H2O2分解的催化效果,某研究小组进行了如下探究:
(1)请写出H2O2分解的化学方程式:2H2O2$\frac{\underline{\;催化剂\;}}{\;}$2H2O+O2↑.
【定性探究】
(2)如图甲,可通过观察产生气泡的速率来定性比较两者的催化效果.
【定量探究】
(3)如图乙,实验前检查该装置的气密性的方法是将注射器活塞向外拉,再松开手活塞又回到原来的位置,则装置气密性良好.要定量比较两者的催化效果,可测量生成等体积气体所需的时间.
【深入探究】
(4)在FeCl3溶液中,究竟是哪种离子起催化作用呢?
猜想1:铁离子(Fe3+)起催化作用;
猜想2:氯离子(Cl-)起催化作用;
…
请设计实验,验证猜想1

(1)请写出H2O2分解的化学方程式:2H2O2$\frac{\underline{\;催化剂\;}}{\;}$2H2O+O2↑.
【定性探究】
(2)如图甲,可通过观察产生气泡的速率来定性比较两者的催化效果.
【定量探究】
(3)如图乙,实验前检查该装置的气密性的方法是将注射器活塞向外拉,再松开手活塞又回到原来的位置,则装置气密性良好.要定量比较两者的催化效果,可测量生成等体积气体所需的时间.
【深入探究】
(4)在FeCl3溶液中,究竟是哪种离子起催化作用呢?
猜想1:铁离子(Fe3+)起催化作用;
猜想2:氯离子(Cl-)起催化作用;
…
请设计实验,验证猜想1
| 实验操作 | 实验现象 | 实验现象 |
| 分别取某体积的同种H2O2溶液于2支试管中,再分别加入等质量的FeCl3和NaCl | 加入FeCl3的试管中产生的气体快,加入NaCl的试管中产生的气体慢 | 猜想1成立 |
10.实验方法能达到实验目的是( )
| 选项 | 实验目的 | 实验方法 |
| A | 除去NaOH溶液中Na2CO3 | 加入适量稀盐酸至不再产生气泡 |
| B | 检验CH4中是否含有CO | 将气体点燃 |
| C | 除去粗盐中的难溶性杂质 | 加入足量水,溶解、蒸发、结晶 |
| D | 比较Fe、Cu、Ag的金属活动性 | 将Fe和Ag分别放入Cu(NO3)2溶液中 |
| A. | A | B. | B | C. | C | D. | D |
 配制50g5%氯化钠溶液.回答问题:
配制50g5%氯化钠溶液.回答问题: