题目内容
14.2016年我市中考化学实验考查的课题为:配制50g质量分数为6%的NaCl溶液.(1)实验步骤包括:
①计算:需要NaCl3.0g,水47.0mL.
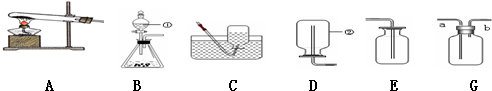
②称量:天平调零后,分别在天平左右托盘放上质量相同的纸片,先,然后,在天平指针略微向右偏移时,可进行操作至天平恰好平衡.
③量取:取用规格为50mL的量筒量取47mL水.
④溶解. 将氯化钠倒入烧杯中,再将量取的水沿烧杯内壁缓缓倒入,并有玻璃棒轻盈均匀搅拌.
(2)下列哪些不当操作会引起溶质质量分数偏小(填序号).
①氯化钠固体仍然不纯 ②称量时砝码端忘垫质量相同的纸片
③溶解食盐的烧杯中残留少量水 ④装瓶时,有少量溶液洒出
(3)溶液的稀释与增浓.
①取1mL6%的NaCl溶液加水稀释至100mL,所得溶液a的溶质质量分数; (由于整个配制过程中溶液很稀,其密度可近似看做1g/mL)
②若将10g15%的NaCl溶液稀释成该浓度的溶液,则需要加入g的水.
③若向50g6%的氯化钠溶液中加入20.0g氯化钠,则溶液的溶质质量分数为.(已知:该温度下,氯化钠的溶解度是36g.计算结果保留一位小数)
分析 (1)①根据称量3g药品的操作分析回答;
(2)若配置得到的氯化钠溶液质量分数偏小,则可能是溶质偏少或溶剂偏多,结合选项分析解答;
(3)根据溶质质量不变及溶液的密度、体积质量之间的关系、溶质质量分数的计算方法分析解答.
解答 解:(1)②用托盘天平称量3.0g的氯化钠,天平调零后,分别在天平左右托盘放上质量相同的纸片,先把游码调至3g位置,然后向左盘中添加药品,在天平指针略微向右偏移时,可用右手轻拍拿药匙的左手手腕至托盘天平恰好平衡;
⑥若配置得到的Na2SO4溶液质量分数偏大,则可能的原因是水量的太少;称量的Na2SO4太多;
(2)若配置得到的氯化钠溶液质量分数偏小,则可能是溶质偏少或溶剂偏多;
①氯化钠固体仍然不纯,导致氯化钠溶质的质量偏少;
②称量时砝码端忘垫质量相同的纸片时,会使称量的氯化钠的质量减小,从而导致溶质质量分数偏小;
③溶解食盐的烧杯中残留少量水,导致溶剂的质量偏多;
④装瓶时,有少量溶液洒出
(3)①取1mL6%的NaCl溶液加水稀释至100mL,溶质的质量不变,设溶质的质量分数为x,则有1mL×6%×1g/mL=100mL×x,解得:x=0.06%;
②若将10g15%的NaCl溶液稀释成该浓度的溶液,设需要加入质量为y的水,则有10g×15%=(10g+y)×6%,解得y=15g;
③该温度下,氯化钠的溶解度是36g,即100g水中最多溶解36g的氯化钠,则50g水中最多溶解18g的氯化钠,所以若向50g6%的氯化钠溶液中加入20.0g氯化钠,不会全部溶解,形成溶液是饱和溶液,据饱和溶液中溶质的质量分数=$\frac{溶解度}{100g+溶解度}$×100%,则溶液中的溶质质量分数为$\frac{36g}{136g}$×100%≈26.5%;
故答案为:
(1)②用镊子移动游码至3g刻度处; 向左盘添加氯化钠固体; 右手轻拍拿药匙的左手手腕;
(2)①②③;
(3)①0.06%;②15; ③26.5%.
点评 本题主要考查了配制一定质量分数溶液的基本操作,溶质的质量分数计算及其相关分析,仪器的正确使用和误差分析等知识,考查知识比较综合,要结合相关知识细心分析解答.

 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案| A化学宏观与微观 | B化学与健康 |
| 物质的构成微粒-分子、原子和离子 碱有共性-碱都含有OH- | 食用新鲜黄瓜-可大量补钙 人体缺铁-易患贫血病 |
| C化学与生活 | D化学与能源 |
| 重金属中毒-喝鲜牛奶、豆浆等解毒 化纤、纯毛织物-用灼烧法来鉴别 | 沼气、酒精-生物能源,可再生能源石油、煤-化石能源,不可再生能源 |
| A. | A | B. | B | C. | C | D. | D |
 NaCl和KNO3两种物质的溶解度曲线如图所示.下列说法正确的是( )
NaCl和KNO3两种物质的溶解度曲线如图所示.下列说法正确的是( )| A. | t1℃时,NaCl的不饱和溶液降温一定会变成饱和溶液 | |
| B. | t2℃时,KNO3溶液降温后一定有晶体析出 | |
| C. | t1℃时,NaCl和KNO3的溶液各100 g,其溶质的质量一定相等 | |
| D. | t2℃时,KNO3饱和溶液中溶质质量分数一定大于NaCl溶液中溶质质量分数 |
| A. | 二氧化碳 | B. | 可吸入颗粒物 | C. | 二氧化硫 | D. | 一氧化碳 |
①金属活动性顺序:M>Cu>Ag
②滤液中一定含有M的阳离子和Cu2+
③金属M可能是Fe
④滤渣中一定含有Ag和Cu
③向滤液中滴加稀盐酸,可能产生白色沉淀
以上说法中正确的是( )
| A. | ①②④ | B. | ②③⑤ | C. | ③④⑤ | D. | ①②⑤ |
| A.解释说明 | B.化学与生活 |
| ①稀有气体作保护气--化学性质稳定 ②O2、CO2化学性质不同--分子构成不同 ③众人拾柴火焰高--可燃物越多,燃烧越旺 | ①蛋白质、油脂、糖类都能为人体提供能量 ②人体所需维生素量不多,但不能缺少 ③玻璃钢、铝合金都是金属材料 |
| C.化学用语中数字的含义 | D.方程式表示所述内容 |
| ①H2O:一个水分子含有两个氢原子 ②$\stackrel{+2}{Ca}$:一个钙离子带有两个单位正电荷 ③$\stackrel{-2}{S}$:硫元素的化合价为负二价 | ①酸雨形成CO2+H2O═H2CO3 ②治疗胃酸过多Al(OH)3 +3HCl═AlCl3+3H2O ③铝制品耐腐的原因:4Al+3O2═2Al2O3 |
| A. | A | B. | B | C. | C | D. | D |
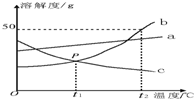 根据如图中a、b、c三种物质的溶解度曲线,回答下列问题:
根据如图中a、b、c三种物质的溶解度曲线,回答下列问题: