题目内容
5. 水是生命的源泉,也是不可缺少的资源.
水是生命的源泉,也是不可缺少的资源.①某矿泉水的主要矿物质成分及含量如下表:
| 成分 | Ca | K | Zn | F |
| 含量(mg/L) | 20 | 3 | 0.06 | 0.02 |
②家用净水机中用活性炭的作用是吸附.
③能确认水是由氧元素和氢元素组成的实验是Ⅰ,Ⅲ(填字母).
Ⅰ.氢气在氧气中燃烧生成水Ⅱ.水的蒸发Ⅲ.水的电解Ⅳ.水的净化
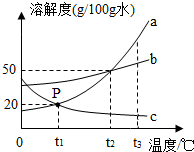
④如图所示是a、b、c三种物质的溶解度曲线,根据图示回答:
Ⅰ.P点的含义是t1℃a和c的溶解度相等,都为20g/100g水.
Ⅱ.t2℃时,将30g a物质加入到50g水中不断搅拌,溶液质量为75g.
Ⅲ.要把t1℃时C物质的不饱和溶液变为饱和溶液,有关说法正确的是AD.
A.可以采取升高温度的方法 B.溶剂的质量一定不变
C.溶质的质量分数一定变大 D.溶质的质量可能不变
Ⅳ.若a溶液中含有少量b,则提纯a的方法是蒸发浓缩、降温结晶.
Ⅴ.将t3℃时将等质量的a、b、c三种物质饱和溶液降温到t1℃时,三种溶液的溶剂质量大小关系是a<b<c.
分析 ①水的主要矿物质中的“Ca、K、Zn、F”等不是以单质、分子、原子等形式存在,而是指元素,通常用元素及其所占质量(质量分数)来描述;
②根据活性炭的作用回答;
③能确认水是由氧元素和氢元素组成的实验要根据质量守恒定律来考虑;
④根据题目信息和溶解度曲线可知:a、b两种固体物质的溶解度,都是随温度升高而增大,而c的溶解度随温度的升高而减少;P点的含义是:t1℃时,a、c的溶解度相等;t2℃时,a的溶解度是50g,因此30ga物质加入到50g水中不断搅拌,形成溶液的质量=25g+50g=75g;要使a从其饱和溶液中析出,可用降温结晶的方法,因为a的溶解度受温度影响变化比较大.
解答 解:①水的主要矿物质中的“Ca、K、Zn、F”等不是以单质、分子、原子等形式存在,而是指元素;
②活性炭有疏松多孔的结构,有很强的吸附性,净水时起到 吸附和过滤的作用;净水器净化后的水中仍含有可溶性的成分,故属于混合物.
③能确认水是由氧元素和氢元素组成的实验要根据质量守恒定律,反应前后元素种类不变,氢气在氧气中燃烧生成水和水通电生成氧气和氢气,都能说明水中含有氢元素和氧元素.
④Ⅰ、由溶解度曲线可知,P点的含义是:t1℃时,a、c的溶解度相等;
Ⅱ.t2℃时,a的溶解度是50g,因此30ga物质加入到50g水中不断搅拌,形成溶液的质量=25g+50g=75g;
Ⅲ.A、C的溶解度随温度的升高而降低,可以采取升高温度的方法变为饱和溶液,故正确;
B、将C的不饱和溶液变为饱和溶液,若采取升温或增加溶质的方法,则溶剂质量不变,故错误;
C、若采取升温变为饱和溶液的方法,溶质的质量分数不变,故错误;
D、若采取升温或蒸发溶剂恰好至饱和的方法,则溶质质量不变,若采取增加溶质的方法,则溶质的质量增加,正确;
Ⅳ.若a溶液中含有少量b,则提纯a的方法是蒸发浓缩、降温结晶;
Ⅴ.将t3℃时a、b、c三种物质为a>b>c,将等质量的a、b、c三种物质饱和溶液降温到t1℃时,三种溶液的溶剂质量大小关系是a<b<c.
答案:
①元素;
②吸附;
③Ⅰ,Ⅲ;
④
Ⅰ.t1℃a和c的溶解度相等,都为20g/100g水;
Ⅱ.75;
Ⅲ.A D;
Ⅳ.蒸发浓缩、降温结晶;
Ⅴ.a<b<c.
点评 本题主要考察了元素、物质的分类、水污染以及水的组成等化学知识,难度不大.考查了溶解度曲线及其应用,通过溶解度曲线我们可以获得很多信息;还考查了有关溶液的计算,有关的计算要准确,本考点主要出现在选择题和填空题中.

| A. |  豆腐切块 | B. |  光合作用 | C. |  烧制茶杯 | D. |  蚕豆制酱 |
| A. | 溶液都是由一种溶质和一种溶剂组成的 | |
| B. | 溶液里各部分的性质是相同的 | |
| C. | 只要条件不变,糖水里的糖不会分离出来 | |
| D. | 通常不指明溶剂的溶液是水溶液 |
| A. | 4P+5O2 $\stackrel{点燃}{→}$ 2P2O5 | B. | C+O2 $\stackrel{点燃}{→}$ CO | ||
| C. | Zn+CuSO4→ZnSO4+Cu | D. | CaCO3+2HCl→CaCl2+CO2↑+H2O |
| A. | 用酚酞鉴别食盐水和稀醋酸 | |
| B. | 用胆矾检验汽油中是否掺水 | |
| C. | 用燃着的木条检验某气体是否是二氧化碳 | |
| D. | 用氯化钡溶液鉴别稀盐酸和稀硫酸 |
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | |
| 溶解度/g | NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
| KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | |
(2)由海水中获取食盐通常采用“海水晒盐”方式获取食盐,由表中数据分析其原因是氯化钠的溶解度受温度影响变化不大;
(3)KNO3和NaCl在某一温度时具有相同的溶解度x,则x的取值范围是20-30℃;
(4)10℃时,分别将35gNaCl和KNO3固体加入100g水中,升温到60℃时,NaCl溶液为不饱和(填“饱和”或“不饱和”)溶液,升温前后有关溶液说法正确的是BC(填序号)
A.10℃时,两溶液中溶质质量分数相同
B.60℃时,两溶液中溶质质量分数相同
C.升温前后,NaCl溶液中溶质质量分数不变
D.升温前后,KNO3溶液中溶质质量分数不变.
| A. | SO2和SO3 | B. | H2S和SO3 | C. | H2S和H2S03 | D. | Na2SO4和SO3 |
 小乐发现切过咸菜的铁质菜刀很容易生锈,她猜测可能是咸菜中的盐水加快了铁的锈蚀,于是它设计了如图所示的实验:
小乐发现切过咸菜的铁质菜刀很容易生锈,她猜测可能是咸菜中的盐水加快了铁的锈蚀,于是它设计了如图所示的实验: