题目内容
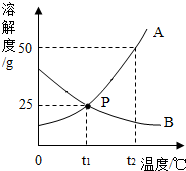 如图是A、B两种固体物质的溶解度曲线.据图回答:
如图是A、B两种固体物质的溶解度曲线.据图回答:(1)P点表示的意义是在t1℃时,A、B两物质的溶解度
(2)把t2℃时等质量A、B两物质的饱和溶液降温到t1℃,析出晶体较多的是
(3)当A中含有少量B物质时,可采用
(4)把t1℃时等质量的A、B两物质的饱和溶液升温到t2℃时,所得溶液中溶质质量分数的大小关系是
(5)t2℃时10克A 物质溶解在
考点:固体溶解度曲线及其作用,结晶的原理、方法及其应用,晶体和结晶的概念与现象,溶质的质量分数、溶解性和溶解度的关系
专题:溶液、浊液与溶解度
分析:(1)根据溶解度曲线的交点表示该温度下两物质的溶解度相等进行解答;
(2)根据A物质的溶解度随温度的降低而减小,B物质的溶解度随温度的降低而增大进行解答;
(3)根据A物质的溶解度随温度的升高而增大进行解答;
(4)根据t1℃时A、B的溶解度相等,且A物质的溶解度随温度的降低而减小,B物质的溶解度随温度的降低而增大进行解答;
(5)根据t2℃时A物质的溶解度为50g进行解答.
(2)根据A物质的溶解度随温度的降低而减小,B物质的溶解度随温度的降低而增大进行解答;
(3)根据A物质的溶解度随温度的升高而增大进行解答;
(4)根据t1℃时A、B的溶解度相等,且A物质的溶解度随温度的降低而减小,B物质的溶解度随温度的降低而增大进行解答;
(5)根据t2℃时A物质的溶解度为50g进行解答.
解答:解:(1)溶解度曲线的交点表示该温度下两物质的溶解度相等,所以P点表示的意义是在t1℃时,A、B两物质的溶解度相等;故填:相等;
(2)A物质的溶解度随温度的降低而减小,B物质的溶解度随温度的降低而增大,所以把t2℃时等质量A、B两物质的饱和溶液降温到t1℃,A会析出晶体,而B不会析出晶体;故填:A;
(3)A物质的溶解度随温度的升高而增大,所以当A中含有少量B物质时,可采用降温结晶的方法提纯A物质;故填:降温;
(4)t1℃时A、B的溶解度相等,所以t1℃时等质量的A、B两物质的饱和溶液的溶质质量分数相同,A物质的溶解度随温度的降低而减小,B物质的溶解度随温度的降低而增大,所以升温到t2℃时,A溶液会变为不饱和溶液,但溶质质量分数不变,而B物质会有晶体析出,溶质质量分数会变小,所以所得溶液中溶质质量分数的大小关系是A>B;故填:A>B;
(5)t2℃时A物质的溶解度为50g,即t2℃时50gA物质溶解在100g水中形成饱和溶液,所以t2℃时10克A物质溶解在20克水中可以恰好形成饱和溶液.所得溶液中溶质的质量分数
×100%=33.3%.故填:20;33.3%.
(2)A物质的溶解度随温度的降低而减小,B物质的溶解度随温度的降低而增大,所以把t2℃时等质量A、B两物质的饱和溶液降温到t1℃,A会析出晶体,而B不会析出晶体;故填:A;
(3)A物质的溶解度随温度的升高而增大,所以当A中含有少量B物质时,可采用降温结晶的方法提纯A物质;故填:降温;
(4)t1℃时A、B的溶解度相等,所以t1℃时等质量的A、B两物质的饱和溶液的溶质质量分数相同,A物质的溶解度随温度的降低而减小,B物质的溶解度随温度的降低而增大,所以升温到t2℃时,A溶液会变为不饱和溶液,但溶质质量分数不变,而B物质会有晶体析出,溶质质量分数会变小,所以所得溶液中溶质质量分数的大小关系是A>B;故填:A>B;
(5)t2℃时A物质的溶解度为50g,即t2℃时50gA物质溶解在100g水中形成饱和溶液,所以t2℃时10克A物质溶解在20克水中可以恰好形成饱和溶液.所得溶液中溶质的质量分数
| 10g |
| 10g+20g |
点评:本题难度不大,主要考查了固体溶解度曲线的意义及根据固体溶解度曲线解决相应的问题,从而培养学生的理解能力和解决问题的能力.

练习册系列答案
相关题目
古诗词是古人为我们留下的宝贵精神财富.下列诗句中没有涉及化学变化的是( )
| A、野火烧不尽,春风吹又生 |
| B、春蚕到死丝方尽,蜡炬成灰泪始干 |
| C、只要功夫深,铁杵磨成针 |
| D、爆竹一声除旧岁,春风送暖入屠苏 |
下列物质主要成分的俗名、名称和化学式不表示同一种物质的是( )
| A、纯碱、碳酸钠、Na2CO3 |
| B、烧碱、氢氧化钠、Na2OH |
| C、消石灰、氢氧化钙、Ca(OH)2 |
| D、小苏打、碳酸氢钠、NaHCO3 |
 在现代生活中,人们越来越注重微量元素的摄取.碘元素对人体有着至关重要的作用.如图是某地市场销售的一种“加碘食盐”包装袋上的部分说明.请回答下列问题:
在现代生活中,人们越来越注重微量元素的摄取.碘元素对人体有着至关重要的作用.如图是某地市场销售的一种“加碘食盐”包装袋上的部分说明.请回答下列问题: