题目内容
配制50g质量分数为6%的氯化钠溶液,下列说法不正确的是( )
| A、用托盘天平称取3g氯化钠固体 |
| B、用规格为50mL的量筒量取水的体积 |
| C、实验步骤是计算、称量(量取)、溶解、装入试剂瓶 |
| D、实验中用到的玻璃仪器只有烧杯和量筒 |
考点:一定溶质质量分数的溶液的配制
专题:溶液、浊液与溶解度
分析:根据溶质质量=溶液质量×溶质的质量分数,溶剂质量=溶液质量-溶质质量,配制50g质量分数为6%的氯化钠溶液的操作步骤分别是:计算、称量、溶解,判断所需要的仪器,据此进行分析判断.
解答:解:A、溶质质量=溶液质量×溶质的质量分数,配制50g质量分数为6%的氯化钠溶液,所需氯化钠的质量为50g×6%=3g;应用托盘天平称取3g氯化钠固体,故选项说法正确.
B、溶剂质量=溶液质量-溶质质量,所需溶剂的质量为50g-3g=47g(合47mL),应用规格为50mL的量筒量取水的体积,故选项说法正确.
C、配制50g质量分数为6%的氯化钠溶液,实验步骤是计算、称量(量取)、溶解、装入试剂瓶,故选项说法正确.
D、配制50g质量分数为6%的氯化钠溶液,首先计算配制溶液所需氯化钠和水的质量,再称量所需的氯化钠和量取水,最后进行溶解;在这些操作中需要的仪器:托盘天平、药匙、量筒、胶头滴管、烧杯和玻璃棒,其中属于玻璃仪器的是玻璃棒、烧杯、胶头滴管、量筒,故选项说法错误.
故选:D.
B、溶剂质量=溶液质量-溶质质量,所需溶剂的质量为50g-3g=47g(合47mL),应用规格为50mL的量筒量取水的体积,故选项说法正确.
C、配制50g质量分数为6%的氯化钠溶液,实验步骤是计算、称量(量取)、溶解、装入试剂瓶,故选项说法正确.
D、配制50g质量分数为6%的氯化钠溶液,首先计算配制溶液所需氯化钠和水的质量,再称量所需的氯化钠和量取水,最后进行溶解;在这些操作中需要的仪器:托盘天平、药匙、量筒、胶头滴管、烧杯和玻璃棒,其中属于玻璃仪器的是玻璃棒、烧杯、胶头滴管、量筒,故选项说法错误.
故选:D.
点评:本题难度不大,明确配制一定溶质质量分数的溶液实验步骤、所需的仪器等是正确解答本题的关键.

练习册系列答案
相关题目
有X,Y,Z三种金属,如果把它们分别放入稀硫酸中,X表面有气泡产生,Y,Z无变化,如果把Y和Z分别放入硝酸银溶液中,过一会儿,在Y表面有银析出,而Z没有变化,根据以上实验事实,判断这三种金属的活动性由强到弱的顺序为( )
| A、X>Y>Z |
| B、Z>Y>Z |
| C、Y>X>Z |
| D、Y>Z>X |
下列关于物质的性质和用途说法不正确的是( )
| A、氧气用于火箭发射,是利用氧气的可燃性 |
| B、氮气用于食品防腐,是利用氮气的化学性质不活泼 |
| C、一氧化碳用于冶金,是利用一氧化碳具有还原性 |
| D、稀有气体充入霓虹灯,是利用稀有气体在通电时能发出不同颜色的光 |
下列行为与“绿色环保”理念不相符的是( )
A、 |
B、 |
C、 |
D、 |
欲探究某混合气体中是否含有CO2、H2O、CO,有如下试剂:①NaOH溶液;②浓H2SO4;③无水CuSO4;④澄清石灰水;⑤灼热的CuO.则气体应依次通过( )
| A、③④①②⑤ | B、②④①⑤ |
| C、③④⑤②① | D、③①④②⑤ |
下图所示实验基本操作错误的是( )
A、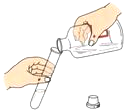 倾倒液体 |
B、 读取液体体积 |
C、 检查气密性 |
D、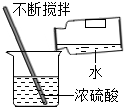 稀释浓硫酸 |
将一瓶稀硫酸分成三等份,分别跟等质量的铝、铁、锌反应后,三种金属都有剩余,且剩余金属的质量为铝>铁>锌,若生成的H2质量分别为a、b、c,则其关系为( )
| A、a>b>c |
| B、c>b>a |
| C、a=b=c |
| D、b>c>a |
