题目内容
3.如图是某化学反应的微观示意图,反应中甲、乙、丙、丁四种分子个数比为2:4:4:1,则从图示获得的信息中正确的是( )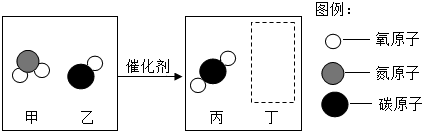
| A. | 甲中氮元素的化合价为+2价 | B. | 乙物质中碳、氧元素的质量比为3:8 | ||
| C. | 丁分子的微观示意图为 | D. | 丙、丁为两种空气中的无毒成分 |
分析 根据化学反应的微观示意图和反应的各物质的微粒数目关系,由质量守恒定律可推出生成物丁,写出反应的化学方程式,据其意义分析判断有关的说法.
解答 解:由化学反应的微观示意图和质量守恒定律可知,生成物丁物质是氮气,反应的化学方程式是:2NO2+4CO$\frac{\underline{\;催化剂\;}}{\;}$4CO2+N2;
A、由上述方程式可知,甲物质是二氧化氮,氮元素的化合价为+4价,故A错误;
B、乙物质是一氧化碳,碳、氧元素的质量比为12:16=3:4.故B错误;
C、丁分子是氮气分子,微观示意图不是 ,故C错误;
,故C错误;
D、丙、丁分别为二氧化碳和氮气,为两种空气中的无毒成分,故D正确.
故选D.
点评 解决这种题的关键就是辨别分子是由何种原子构成,每种原子有几个,这样就可以得出分子的化学式,再利用化学方程式对相关知识进行分析判断即可.

练习册系列答案
相关题目
14.对有关实验现象的描述正确的是( )
| A. | 碳在氧气中燃烧发出白光 | B. | 硫在氧气中燃烧发出淡蓝色的火焰 | ||
| C. | 铁丝在氧气中燃烧生成四氧化三铁 | D. | 磷在空气中燃烧放出白雾 |
18.下列有关资源、能源的叙述错误的是( )
| A. | 空气中含量最多的单质是氮气 | |
| B. | 按目前测定,海水中含量最多的元素是氧元素 | |
| C. | 煤、石油、沼气、风能等都是可再生能源 | |
| D. | 防止金属腐蚀是保护金属资源的有效途径 |
8.氢气是21世纪极有前途的新型能源,是各国研究的热点之一,如何制取和安全高效使用氢气,是课题的关键,以下研究方向中你认为不可行的是( )
| A. | 寻找特殊材料,安全高效储存氢气 | |
| B. | 设法将太阳能聚焦,产生高温使水分解产生氢气 | |
| C. | 寻找更多的化石燃料,利用其燃烧放热,使水分解产生氢气 | |
| D. | 寻找新型催化剂,常温下分解水制取氢气 |
15.下列有关概念应用的举例正确的是( )
| A. | CO2、Fe2O3、H2SO4、O2等都含氧元素,都属于氧化物 | |
| B. | 生铁含碳量2%~4.3%,钢含碳量0.03%~2% | |
| C. | 可燃物与氧气发生的反应都是剧烈的化合反应 | |
| D. | 凡是生成盐和水的反应都是中和反应 |
3. 某学习小组对课本中“食盐常用于制氧气、烧碱”的内容产生兴趣.在老师的指导下,用自制的实验装置(主要部分如图所示)进行电解饱和食盐水制取氢氧化钠的实验.一段时间后,关闭电源,从K处导出部分的溶液作为待测液进行如下研究.
某学习小组对课本中“食盐常用于制氧气、烧碱”的内容产生兴趣.在老师的指导下,用自制的实验装置(主要部分如图所示)进行电解饱和食盐水制取氢氧化钠的实验.一段时间后,关闭电源,从K处导出部分的溶液作为待测液进行如下研究.
老师提示:
I.电解饱和食盐水的化学方程式:
2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑
Ⅱ.忽略其他可能发生的反应对本实验的影响.
探究活动一:检验待测液中含有氢氧化钠
(1)同学们选用某种酸碱指示剂对待测液进行检验,请你将实验报告填写完整.
探究活动二:测定待测液中氢氧化钠的质量分数
【实验】用沉淀法测定
资料摘要:氢氧化钠与氯化镁在溶液中发生反应:
同学们按如图所示的实验步骤进行实验:
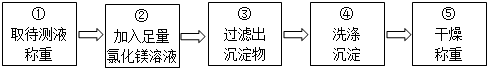
(2)步骤②加入的氯化镁溶液必需足量,其目的是使氢氧化钠完全反应.步骤④中判断沉淀物是否洗净的具体操作:取最后一次洗涤液少许于试管中,滴加硝酸银溶液,如果不产生白色沉淀,说明已经洗净,如果产生白色沉淀,说明没有洗净(写出实验步骤、现象和结论).
(5)步骤②中发生反应的化学方程式是2NaOH+MgCl2=Mg(OH)2↓+2NaCl.
(6)利用沉淀物的质量计算氢氧化钠的质量分数,若缺少步骤④的操作,所测定氢氧化钠的质量分数将偏大(选填“偏大”、“偏小”或“没影响”).
 某学习小组对课本中“食盐常用于制氧气、烧碱”的内容产生兴趣.在老师的指导下,用自制的实验装置(主要部分如图所示)进行电解饱和食盐水制取氢氧化钠的实验.一段时间后,关闭电源,从K处导出部分的溶液作为待测液进行如下研究.
某学习小组对课本中“食盐常用于制氧气、烧碱”的内容产生兴趣.在老师的指导下,用自制的实验装置(主要部分如图所示)进行电解饱和食盐水制取氢氧化钠的实验.一段时间后,关闭电源,从K处导出部分的溶液作为待测液进行如下研究.老师提示:
I.电解饱和食盐水的化学方程式:
2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑
Ⅱ.忽略其他可能发生的反应对本实验的影响.
探究活动一:检验待测液中含有氢氧化钠
(1)同学们选用某种酸碱指示剂对待测液进行检验,请你将实验报告填写完整.
| 实验步骤 | 实验现象 | 实验结论 |
| 待测液呈碱性,表明含有氢氧化钠. |
【实验】用沉淀法测定
资料摘要:氢氧化钠与氯化镁在溶液中发生反应:
同学们按如图所示的实验步骤进行实验:

(2)步骤②加入的氯化镁溶液必需足量,其目的是使氢氧化钠完全反应.步骤④中判断沉淀物是否洗净的具体操作:取最后一次洗涤液少许于试管中,滴加硝酸银溶液,如果不产生白色沉淀,说明已经洗净,如果产生白色沉淀,说明没有洗净(写出实验步骤、现象和结论).
(5)步骤②中发生反应的化学方程式是2NaOH+MgCl2=Mg(OH)2↓+2NaCl.
(6)利用沉淀物的质量计算氢氧化钠的质量分数,若缺少步骤④的操作,所测定氢氧化钠的质量分数将偏大(选填“偏大”、“偏小”或“没影响”).