题目内容
19.下列实验现象的描述中,正确的是( )| A. | 打开盛放浓盐酸的试剂瓶盖,瓶口有大量白烟产生 | |
| B. | 铁锈与稀盐酸完全反应后,溶液由无色变成浅蓝色 | |
| C. | 硫在氧气中燃烧,发出淡蓝色的火焰,放出大量的热 | |
| D. | 将过量的盐酸滴入含有石蕊的氢氧化钠溶液中,溶液由蓝色变成红色 |
分析 A、考虑浓盐酸易挥发,在空气中容易形成白雾;
B、考虑氯化亚铁溶液是浅绿色的,氯化铁溶液是黄色的;
C、考虑硫在空气中燃烧时发出淡蓝色火焰,而在氧气中燃烧时发出明亮的蓝紫色火焰;
D、考虑石蕊遇酸碱变色的规律.
解答 解:A、打开浓盐酸试剂瓶的瓶塞,瓶口上方出现大量白雾,是氯化氢气体和空气中的水蒸气结合成盐酸小液滴的缘故.故不正确.
B、铁锈的主要成分是氧化铁,与稀盐酸反应能生成氯化铁和水,氯化铁溶液是黄色的.故不正确.
C、硫在氧气中燃烧发出明亮的蓝紫色火焰.故不正确.
D、将过量的盐酸滴入含有石蕊的氢氧化钠溶液中,溶液由蓝色变成红色,故说法正确.
故选:D.
点评 化学实验现象是化学实验最突出、最鲜明的部分,也是进行分析推理得出结论的依据,掌握物质的性质和相互之间的反应关系,并有助于提高观察、实验能力.所以,对化学实验不仅要认真观察,还应掌握观察实验现象的方法.

练习册系列答案
相关题目
10.下列图象不能正确反映对应变化关系的是( )
| A. | 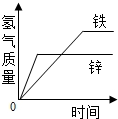 将颗粒大小相同质量相同的铁和锌分别加入到足量的同质量、同质量分数的稀盐酸中 | |
| B. | 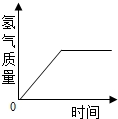 向一定量的稀硫酸中不断加入锌粒 | |
| C. | 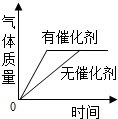 用两份等质量、等浓度的过氧化氢溶液分别制取氧气,生成气体质量的变化 | |
| D. | 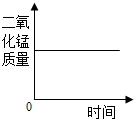 加热高锰酸钾制氧气,生成二氧化锰质量的变化 |
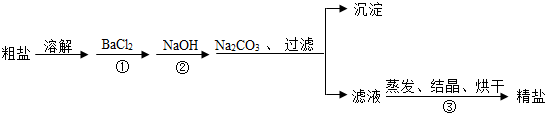
7. 安多夫是一种嫩肉粉,其主要成分碳酸氢钠(NaHCO3)可破坏肉质纤维结构、促进肉类吸收水分,从而使肉质松软,达到鲜嫩爽滑的目的.小于发现将拌了安多夫粉的肉类放到锅中并加入食醋等调料烧煮时产生了大量气体,他对此颇感兴趣,决定对其进行探究.
安多夫是一种嫩肉粉,其主要成分碳酸氢钠(NaHCO3)可破坏肉质纤维结构、促进肉类吸收水分,从而使肉质松软,达到鲜嫩爽滑的目的.小于发现将拌了安多夫粉的肉类放到锅中并加入食醋等调料烧煮时产生了大量气体,他对此颇感兴趣,决定对其进行探究.
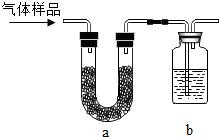
(1)小于对气体的成分进行了猜测:气体中除了醋酸气体之外,还可能含有水蒸气和CO2,他设法收集气体样品并除去醋酸气体后,用如图实验装置进行验证,装置a中盛放的试剂是无水硫酸铜.
(2)小于对二氧化碳的来源作了两种猜测:
猜测①:可能是醋酸与碳酸氢钠反应生成的;
猜测②:二氧化碳可能是由碳酸氢钠受热分解产生的.
针对以上猜测,小于设计了以下实验:
实验结论:猜想①、②都正确.
(3)实验2中,小于发现充分反应后,试管中仍留有一些白色粉末,他猜测可能是氢氧化钠或碳酸钠,请用物理、化学方法各1种进行鉴别.
①物理方法:各取少量溶于水放热的是氢氧化钠.
②化学方法:加入氯化钙有沉淀产生的是碳酸钠.
 安多夫是一种嫩肉粉,其主要成分碳酸氢钠(NaHCO3)可破坏肉质纤维结构、促进肉类吸收水分,从而使肉质松软,达到鲜嫩爽滑的目的.小于发现将拌了安多夫粉的肉类放到锅中并加入食醋等调料烧煮时产生了大量气体,他对此颇感兴趣,决定对其进行探究.
安多夫是一种嫩肉粉,其主要成分碳酸氢钠(NaHCO3)可破坏肉质纤维结构、促进肉类吸收水分,从而使肉质松软,达到鲜嫩爽滑的目的.小于发现将拌了安多夫粉的肉类放到锅中并加入食醋等调料烧煮时产生了大量气体,他对此颇感兴趣,决定对其进行探究.(1)小于对气体的成分进行了猜测:气体中除了醋酸气体之外,还可能含有水蒸气和CO2,他设法收集气体样品并除去醋酸气体后,用如图实验装置进行验证,装置a中盛放的试剂是无水硫酸铜.
(2)小于对二氧化碳的来源作了两种猜测:
猜测①:可能是醋酸与碳酸氢钠反应生成的;
猜测②:二氧化碳可能是由碳酸氢钠受热分解产生的.
针对以上猜测,小于设计了以下实验:
| 实验步骤 | 实验现象 | |
| 实验1 | 取碳酸氢钠样品少许加入试管中,加入少量醋酸使之充分反应,并把生的气体通入澄清石灰水 | 有气泡产生,石灰水变浑浊 |
| 实验2 | 取碳酸氢钠样品少许加入试管中,加热使之充分反应,并把产生的气体通入澄清石灰水中 | 试管口出现小水珠,澄清石灰水变浑浊 |
(3)实验2中,小于发现充分反应后,试管中仍留有一些白色粉末,他猜测可能是氢氧化钠或碳酸钠,请用物理、化学方法各1种进行鉴别.
①物理方法:各取少量溶于水放热的是氢氧化钠.
②化学方法:加入氯化钙有沉淀产生的是碳酸钠.
14.如图所示实验基本操作不正确的是( )
| A. | 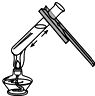 给盛有液体的试管加热 | B. |  向试管中加入液体 | ||
| C. |  闻药品气味 | D. | 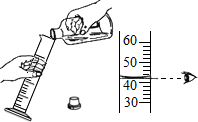 量取液体体积 |
11.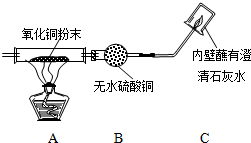 某混合气体中可能含有H2、CO、CO2中的几种,现将此气体分别通过A、B、C装置,A装置中的粉末变红色,B装置中的粉末变蓝色,C装置中烧杯的内壁变白色浑浊,下列判断不正确的是( )
某混合气体中可能含有H2、CO、CO2中的几种,现将此气体分别通过A、B、C装置,A装置中的粉末变红色,B装置中的粉末变蓝色,C装置中烧杯的内壁变白色浑浊,下列判断不正确的是( )
 某混合气体中可能含有H2、CO、CO2中的几种,现将此气体分别通过A、B、C装置,A装置中的粉末变红色,B装置中的粉末变蓝色,C装置中烧杯的内壁变白色浑浊,下列判断不正确的是( )
某混合气体中可能含有H2、CO、CO2中的几种,现将此气体分别通过A、B、C装置,A装置中的粉末变红色,B装置中的粉末变蓝色,C装置中烧杯的内壁变白色浑浊,下列判断不正确的是( )| A. | 可能是H2和CO | B. | 可能是CO和CO2 | ||
| C. | 可能是H2、CO和CO2 | D. | 可能是H2和CO2 |
8.某校兴趣小组承担了某项研究课题的一部分:通过实验探究气体X(已知含两种元素)的元素组成.实验装置如图所示.将0.17gX气体由注射器A缓缓送入B装置(B装置中的空气已预先除去),使之完全反应,生成的气体全部用D装置抽取收集.实验现象和数据记录如表:
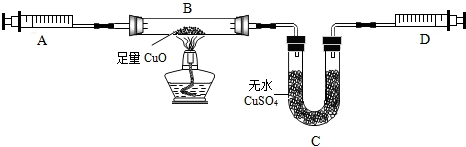
(1)X中一定有氢元素.
(2)经测定,D中的气体由一种元素组成,常温常压下密度是1.25g/L,试推测该气体的化学式是N2,其质量是0.14g.(常见气体密度如下)

| 现 象 | 反应前质量(g) | 反应后质量(g) | |
| B装置中 | 逐渐变成亮红色 | 21.32 | 21.08 |
| C装置中 | 变蓝色 | 32.16 | 32.43 |
(2)经测定,D中的气体由一种元素组成,常温常压下密度是1.25g/L,试推测该气体的化学式是N2,其质量是0.14g.(常见气体密度如下)
| 气 体 | H2 | O2 | CO | CH4 | N2 | CO2 |
| 常温常压时的密度(g/L) | 0.09 | 1.43 | 1.25 | 0.72 | 1.25 | 1.98 |
9.下列做法与节能减排的低碳生活不相符的是( )
| A. | 冬季将室内空调温度设置最高 | |
| B. | 城市照明系统大力推广利用太阳能 | |
| C. | 拒绝使用一次性筷子 | |
| D. | 利用秸秆、粪便等制成沼气来替代化石燃料 |
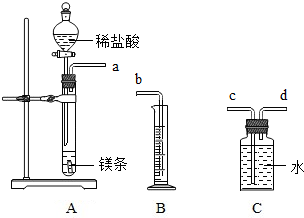 请利用如图给定的仪器组装成一套测定镁的相对原子质量的实验装置(每种仪器只允许使用一次),用排水法测量化学反应产生氢气的体积,根据化学方程式计算出镁的相对原子质量,回答问题:
请利用如图给定的仪器组装成一套测定镁的相对原子质量的实验装置(每种仪器只允许使用一次),用排水法测量化学反应产生氢气的体积,根据化学方程式计算出镁的相对原子质量,回答问题: