题目内容
16.电石的化学名称是碳化钙(CaC2),不可燃,是一种有机合成化学工业的基本原料,化学性质非常活泼,遇水后能激烈分解产生乙炔(C2H2)气体和氢氧化钙,释放出大量的热,请用你学过的知识回答以下问题:(1)请写出碳化钙遇水后的化学方程式CaC2+2H2O=C2H2↑+Ca(OH)2;
(2)根据上述信息,你认为应该如何保存电石?并简述理由.密封防水.
分析 (1)碳化钙(CaC2)遇水后能激烈分解产生乙炔(C2H2)气体和氢氧化钙,写出反应的化学方程式即可.
(2)根据题意可知,电石(CaC2)不可燃,化学性质非常活泼,与水接触剧烈反应产生乙炔,乙炔是可燃物,进行分析解答.
解答 解:(1)碳化钙(CaC2)遇水后能激烈分解产生乙炔(C2H2)气体和氢氧化钙,反应的化学方程式为:CaC2+2H2O=C2H2↑+Ca(OH)2.
(2)电石(CaC2)不可燃,化学性质非常活泼,与水接触剧烈反应产生乙炔,生成的乙炔是可燃物,为了保证安全,故保存电石时应注意密封防水.
故答案为:(1)CaC2+2H2O=C2H2↑+Ca(OH)2;(2)密封防水.
点评 本题难度不大,掌握化学方程式的书写方法、碳化钙能与水反应生成可燃性气体等并能灵活运用是正确解答本题的关键.

练习册系列答案
相关题目
7.下列物质的鉴别方法不正确的是( )
| A. | 用稀硫酸鉴别木炭粉和铁粉 | |
| B. | 用带火星的木条鉴别二氧化碳和氮气 | |
| C. | 用肥皂水鉴别氯化钙溶液和氯化钠溶液 | |
| D. | 用水鉴别碳酸钙粉末和碳酸钠粉末 |
8.我国科学家屠呦呦因为发现青蒿素,获得2015年诺贝尔医学奖.青蒿素是治疗疟疾的特效药,化学式可表示为C15H22O5,下列关于青蒿素的说法正确的是( )
| A. | 青蒿素含有42个原子 | B. | 青蒿素属于氧化物 | ||
| C. | 青蒿素中C、H、O的质量比是15:22:5 | D. | 青蒿素中碳元素质量分数最高 |
 碳及其化合物在生产、生活中应用广泛.
碳及其化合物在生产、生活中应用广泛.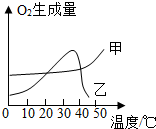 实验室常用二氧化锰催化分解过氧化氢的方法制取氧气,请写出反应的化学方程式:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.某同学从课外读物中得知新鲜的动物肝脏中有较多的过氧化氢酶,过氧化氢酶与无机催化剂Fe3+都可以催化过氧化氢分解.
实验室常用二氧化锰催化分解过氧化氢的方法制取氧气,请写出反应的化学方程式:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.某同学从课外读物中得知新鲜的动物肝脏中有较多的过氧化氢酶,过氧化氢酶与无机催化剂Fe3+都可以催化过氧化氢分解.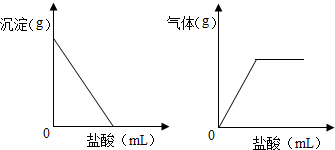 有一包白色固体,可能含有硫酸钠、碳酸钠、氯化钡、氢氧化钠中的一种或几种,取样溶于水,有白色沉淀产生;过滤后向沉淀中滴加盐酸,沉淀的量、产生气体的量与加入盐酸体积的关系如图所示,由此推断白色固体中一定存在Na2CO3、BaCl2,一定不存在Na2SO4(均填写化学式).
有一包白色固体,可能含有硫酸钠、碳酸钠、氯化钡、氢氧化钠中的一种或几种,取样溶于水,有白色沉淀产生;过滤后向沉淀中滴加盐酸,沉淀的量、产生气体的量与加入盐酸体积的关系如图所示,由此推断白色固体中一定存在Na2CO3、BaCl2,一定不存在Na2SO4(均填写化学式).