题目内容
14.有CO、CO2两瓶无声气体,请用两种方法检验它们,简述所用试剂、操作结论.分析 根据CO与CO2的不同性质进行检验:一氧化碳有可燃性,还原性,二氧化碳没有;二氧化碳能使石灰水变浑浊,溶于水后能使紫色石蕊试液变红色,一氧化碳不能,
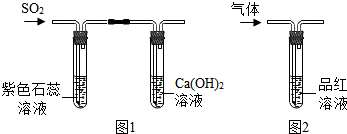
解答 解:可将两种气体分别通入澄清石灰水、紫色石蕊试液、灼热的氧化铜中,根据不同现象得出结论.
故答案为:(1)将两种气体分别通入澄清石灰水,使石灰水变混浊的为CO2;
(2)将两种气体分别通过灼热的氧化铜,使固体由黑色变成红色的是CO;(或将两种气体分别通入紫色石蕊试液,石蕊试液变红色,说明通入的为CO2,合理即可).
点评 此题主要是考查同学们的综合分析能力,不但要求同学们具备有关物质的基础知识,而且要有实验操作的经历和分析、解决化学实验问题的能力.解题时需要认真分析题目给出的条件,联系实际,逐一分析推断.

练习册系列答案
相关题目
4.化学方程式是世界通用的化学语言,正确的化学方程式是( )
| A. | 4Fe+3O2$\stackrel{点燃}{→}$2Fe2O3 | B. | CO+CuO$\stackrel{△}{→}$Cu+CO2↑ | ||
| C. | 2H2O$\stackrel{通电}{→}$2H2↑+O2↑ | D. | BaCl2+2NaNO3→Ba(NO3)2+2NaCl |
5.应用守恒思想,推论正确的是( )
| A. | 50mL酒精中加入50mL水,则酒精溶液的体积为100毫升 | |
| B. | 聚乙烯燃烧生成二氧化碳和水,则聚乙烯一定由碳、氢、氧元素组成 | |
| C. | 1mol硫与1mol氧气充分反应,则生成二氧化硫的物质的量为2mol | |
| D. | 某纯净物燃烧生成CO2和H2O分子个数比为2:3,则该纯净物分子中C、H原子个数比为1:3 |
2.实验室测定菱铁矿主要成分的含量时,取29g含杂质的菱铁矿(杂质不溶于水也不与酸反应)加入到200g稀盐酸中,恰好完全反应,过滤得滤液214.4g,则该菱铁矿主要成分的质量分数为( )
| A. | 75% | B. | 80% | C. | 85% | D. | 90% |
19.不另选试剂,仅用组内物质间的相互反应,不能将它们鉴别出来的是( )
| A. | FeCl3 NaOH NaCl H2SO4 | B. | HCl CuSO4 KOH NaNO3 | ||
| C. | AgNO3 HCl NaCl HNO3 | D. | BaCl2 Na2SO4 Na2CO3 HCl |
6.关于2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑的读法,正确的是( )
| A. | 水在通电条件下,分解为氢元素和氧元素 | |
| B. | 每2个水分子等于2个氢分子和氧分子 | |
| C. | 水在通电条件下,分解为氢气加氧气 | |
| D. | 水在通电条件下,分解为氢气和氧气 |
14.表示两个氧分子的是( )
| A. | 2O | B. | 2O2 | C. | O | D. | O2 |
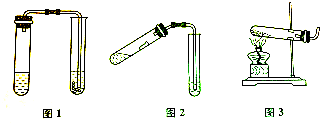 (1)第一次实验:取一小段镁条放入试管中,然后加入适量的稀硫酸.连接好装置如图1.是澄清石灰水没有变浑浊,分析原因可能是由于石灰水变质,导致现状不明;
(1)第一次实验:取一小段镁条放入试管中,然后加入适量的稀硫酸.连接好装置如图1.是澄清石灰水没有变浑浊,分析原因可能是由于石灰水变质,导致现状不明;