题目内容
13.除去CO中混有少量的CO2,可将混合气体通入足量的氢氧化钠溶液,也可将混合气体通过足量的炽热的碳层;除去CO2 中混有的CO,可将混合气体通过足量的灼热的氧化铜.分析 根据二氧化碳可被碱溶液吸收和二氧化碳与一氧化碳的相互转化方法进行分析解答.
解答 解:二氧化碳可以被碱溶液吸收,而一氧化碳与碱溶液不反应,故可以用碱溶液来除去一氧化碳中的二氧化碳,故填:氢氧化钠溶液;
二氧化碳在高温条件下与碳反应可以生成一氧化碳,故可将混合气体通过足量的炽热的碳层,使一氧化碳中的二氧化碳杂质转变成一氧化碳,而被除去,故填:碳层;
一氧化碳在加热条件下与氧化铜反应可以生成二氧化碳,故填:氧化铜.
点评 在解此类题时,首先分析杂质和物质的性质,然后选择适当的试剂只与杂质反应,不与主要物质反应,不会生成新的杂质,此题要注意二氧化碳中有一氧化碳杂质不能用点燃的方法除去,因为二氧化碳不支持燃烧,其中少量的一氧化碳是不能被点燃的.

练习册系列答案
 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案
相关题目
3.下列物质在应用中,只应用其化学性质的是( )
| A. | 用铅笔芯粉末使锁的开启变的更灵活 | |
| B. | 将活性炭放入冰箱中除去异味 | |
| C. | 用二氧化碳灭火 | |
| D. | 用一氧化碳来冶炼生铁 |
1.某同学做了如图所示的实验并记录数据如下:

(1)实验中生成银的化学方程式有Fe+2AgNO3═Fe(NO3)2+2Ag,Cu+2AgNO3═Cu(NO3)2+2Ag;
(2)实验2后滤渣的成分为银、铜;
(3)求实验1中铁所置换出的银质量(x)的比例式为$\frac{56}{2.8g}$=$\frac{216}{x}$;
(4)用硝酸银固体配制实验中所需的硝酸银溶液,需要水的质量为149g;
(5)向实验3所得滤液中加入16g水,此时溶液中溶质的质量分数为18.4%.

| 硝酸银溶液的质量 | 铜粉的质量 | 铁粉的质量 | 所得滤渣的质量 | |
| 实验1 | 200g | 3.2g | 2.8g | 21.6g |
| 实验2 | 200g | 4.8g | 2.8g | 23.2g |
| 实验3 | 200g | 3.2g | 5.6g | 24.8g |
| 实验4 | 200g | 4.8g | 5.6g | 26.4g |
(2)实验2后滤渣的成分为银、铜;
(3)求实验1中铁所置换出的银质量(x)的比例式为$\frac{56}{2.8g}$=$\frac{216}{x}$;
(4)用硝酸银固体配制实验中所需的硝酸银溶液,需要水的质量为149g;
(5)向实验3所得滤液中加入16g水,此时溶液中溶质的质量分数为18.4%.
8.下列各组物质中前者为化合物,后者为混合物的是( )
| A. | 铁、钢 | B. | 蒸馏水、空气 | C. | 水银、液氧 | D. | 白磷、冰水混合物 |
5.化学是一门以实验为基础的科学,实验必须按照一定规则进行.下列实验的操作先后顺序不正确的是( )
| A. | 点燃可燃性气体前,应先检验气体的纯度,后点燃 | |
| B. | 实验室用高锰酸钾制氧气实验结束时,应先熄灭酒精灯,后将导管移出水面 | |
| C. | 实验室制取O2、H2等气体时,应先检查装置气密性,再向容器中装药品 | |
| D. | 浓硫酸的稀释时,应先在烧杯中放入适量的水,再沿着烧杯壁缓缓倒入浓硫酸 |
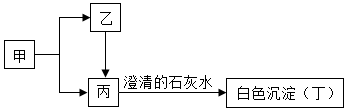 甲、乙、丙、丁是初中化学常见物质,其中甲是单质,乙、丙是组成元素完全相同的两种气体,它们相互转化的关系如图(部分反应物或生成物及反应条件略).
甲、乙、丙、丁是初中化学常见物质,其中甲是单质,乙、丙是组成元素完全相同的两种气体,它们相互转化的关系如图(部分反应物或生成物及反应条件略).