题目内容
1.由C3H6O2和C5H10组成的混合物中,若含氧元素的质量分数为30%,则其中氢元素的质量分数为( )| A. | 8% | B. | 20% | C. | 12% | D. | 10% |
分析 根据C5H10、C3H6O两种物质的化学式,可发现两种物质中C、H元素质量比都为12:2=6:1,因此混合物中C、H元素的质量比也为6:1;根据混合物中只含C、H、O三种元素,因此1-30%=70%即混合物中C、H元素的质量分数和;综合以上分析,计算出混合物氢元素质量分数.
解答 解:根据C5H10、C3H6O两种物质的化学式,可发现两种物质中C、H元素质量比都为12:2=6:1,因此混合物中C、H元素的质量比也为6:1;根据混合物中只含C、H、O三种元素,因此1-30%=70%即混合物中C、H元素的质量分数和;故碳元素的质量分数为70%×$\frac{1}{7}$=10%;
故选:D.
点评 发现两种物质中C、H元素质量比相等是解决本问题的技巧与关键,此类问题中元素的质量分数往往有一定的特殊关系.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
12.某校的研究性学习小组进行测定混合物各组分质量比的研究,甲、乙、丙三位同学各设计了一种实验方案如下表所示:(混合物的质量事先已称量好)
试回答下列问题:
(1)你认为甲同学设计的实验步骤中,根据称量所得到的数据,不能(填“能”或“不能”)准确计算出混合物中各组分的质量比.
(2)经讨论大家认为,乙同学所设计的实验步骤的第四步填写一定有错误.其原因是什么?晶体中还还含有碳酸钠.
(3)丙同学对实验进行了较合理的设计,仿照前面的形式,第三步和第五步的对应的空格内应填上的内容是称量过滤干燥后氢氧化镁固体质量.
| 实验 序号 | 混合物 | 第一步:加入适量水,充分溶解 | 第二步:加入或通入的试剂 | 第三步:过滤后洗涤干燥所得固体 | 第四步:蒸发滤液得到晶体 | 第五步:称量,记录数据计算质量比 |
| 甲 | BaCl2 NaCl | 澄清溶液 | 过量CO2 | 无固体 | 晶体 | 称量所得 晶体 |
| 乙 | CaCl2 NaCl | 澄清溶液 | 过量饱和 Na2CO3溶液 | CaCO3 | NaCl | 称量蒸发 所得晶体 |
| 丙 | Na2SO4 MgSO4 | 澄清溶液 | 过量NaOH 溶液 | 略 |
(1)你认为甲同学设计的实验步骤中,根据称量所得到的数据,不能(填“能”或“不能”)准确计算出混合物中各组分的质量比.
(2)经讨论大家认为,乙同学所设计的实验步骤的第四步填写一定有错误.其原因是什么?晶体中还还含有碳酸钠.
(3)丙同学对实验进行了较合理的设计,仿照前面的形式,第三步和第五步的对应的空格内应填上的内容是称量过滤干燥后氢氧化镁固体质量.
9.为探究NaCl和CuSO4对唾液淀粉酶活性的影响,某同学进行了实验,实验步骤和结果见表.请回答:
(1)实验中加入缓冲液的作用是维持反应液中pH的稳定.
(2)分析实验结果可知:对酶活性有影响的离子是Cl-和Cu2+,其中对酶活性有抑制作用的离子是Cu2+,对酶活性有促进作用的离子是Cl-.
(3)该实验中设置4号试管的目的是对照;设置3号试管的目的是确定Na+和SO42-对唾液淀粉酶催化活性是否有影响.
| 试管编号 实验步骤 | 1 | 2 | 3 | 4 |
| 1%NaCl溶液(mL) | 1 | |||
| 1% CuSO4溶液(mL) | 1 | |||
| 1% Na2SO4溶液(mL) | 1 | |||
| 蒸馏水(mL) | 1 | |||
| pH6.8缓冲液(mL) | 1 | 1 | 1 | 1 |
| 1%淀粉溶液(mL) | 1 | 1 | 1 | 1 |
| 唾液淀粉酶溶液(mL) | 1 | 1 | 1 | 1 |
| 各试管放入37℃恒温水浴保温适宜时间 | ||||
| 取出试管,加入1%碘溶液0.1mL | ||||
| 观察结果 | 无色 | 深蓝色 | 浅蓝色 | |
(2)分析实验结果可知:对酶活性有影响的离子是Cl-和Cu2+,其中对酶活性有抑制作用的离子是Cu2+,对酶活性有促进作用的离子是Cl-.
(3)该实验中设置4号试管的目的是对照;设置3号试管的目的是确定Na+和SO42-对唾液淀粉酶催化活性是否有影响.
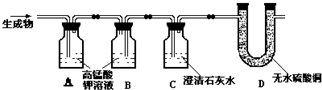
 化学是一门以实验为基础的科学,请回答下列问题:
化学是一门以实验为基础的科学,请回答下列问题: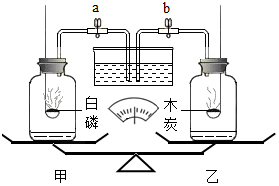 将等容积等质量(包括瓶塞、导管、燃烧匙)的两集气瓶置于天平左右两盘,并调至平衡,然后分别放入等质量的白磷和木炭,如下图所示,关闭止水夹a、b,使二者充分燃烧,冷却至室温后,打开止水夹a、b.
将等容积等质量(包括瓶塞、导管、燃烧匙)的两集气瓶置于天平左右两盘,并调至平衡,然后分别放入等质量的白磷和木炭,如下图所示,关闭止水夹a、b,使二者充分燃烧,冷却至室温后,打开止水夹a、b.