题目内容
3.用化学符号表示:(1)5个氨根离子5NH4+
(2)三个磷原子3P
(3)负2价的氧元素$\stackrel{-2}{O}$
(4)标出氯化镁中镁元素的化合价$\stackrel{+2}{Mg}$Cl2
(5)两个氮分子2N2
(6)2个铝离子2Al3+.
分析 本题考查化学用语的意义及书写,解题关键是分清化学用语所表达的对象是分子、原子、离子还是化合价,才能在化学符号前或其它位置加上适当的计量数来完整地表达其意义,并能根据物质化学式的书写规则正确书写物质的化学式,才能熟练准确的解答此类题目.
解答 解:(1)离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其元素符号前加上相应的数字,故5个铵根离子可表示为:5NH4+;
(2)原子的表示方法就是用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字.所以三个磷原子,就可表示为:3P;
(3)元素化合价的表示方法:确定出化合物中所要标出的元素的化合价,然后在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后,所以负2价的氧元素,故可表示为:$\stackrel{-2}{O}$;
(4)元素化合价的表示方法:确定出化合物中所要标出的元素的化合价,然后在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后,所以标出氯化镁中镁元素的化合价,故可表示为:$\stackrel{+2}{Mg}$Cl2;
(5)由分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字,则两个氮分子可表示为:2N2;
(6)由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其离子符号前加上相应的数字,故2个铝离子可表示为:2Al3+;
故答案为:(1)5NH4+;(2)3P;(3)$\stackrel{-2}{O}$;(4)$\stackrel{+2}{Mg}$Cl2;(5)2N2;(6)2Al3+;
点评 本题主要考查学生对化学用语的书写和理解能力,题目设计既包含对化学符号意义的了解,又考查了学生对化学符号的书写,考查全面,注重基础,题目难度较易.

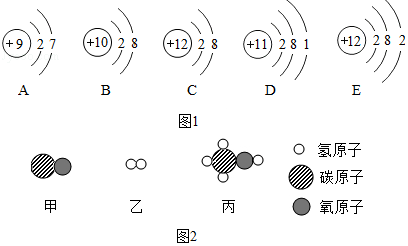
| A. | 原子能构成分子,但不能直接构成物质 | |
| B. | 分子由原子构成,原子不能再分 | |
| C. | 分子是保持物质化学性质的一种微粒 | |
| D. | 固体难压缩,说明固体分子间无间隔 |
【猜想与假设】
①氢氧化钠没有变质;②该氢氧化钠部分变质;③该氢氧化钠全部变质.
【设计实验】取氢氧化钠固体样品溶于水配成溶液A,进行如下实验:
| 实验步骤 | 实验现象 | 结论及解释 |
| (1)取少量溶液A于试管中,向其中滴加足量的稀盐酸 | 有气泡产生 | 猜想①不成立 |
| (2)另取少量溶液A于试管中,向其中滴加足量的氯化钙溶液 | 产生白色沉淀 | 反应的化学方程式为Na2CO3+CaCl2=CaCO3↓+2NaCl |
| (3)将步骤(2)所得的混合液静置,向上层清液中滴加无色的酚酞溶液 | 溶液呈红色 | 猜想②成立 |
(4)久置的氢氧化钠变质的原因是(用化学方程式表示)CO2+2NaOH=Na2CO3+H2O.
【探索与拓展】(5)为进一步探究氢氧化钠的变质程度,小明称取18.6g氢氧化钠固体样品放入烧杯中,向其中逐滴加入稀盐酸,到不再产生气泡为止,共消耗稀盐酸100g,反应后称得烧杯中溶液的质量为115.6g.求该样品中碳酸的质量分数(要写出计算过程).
 某兴趣小组为验证质量守恒定律,除了镁条在空气中燃烧的实验.
某兴趣小组为验证质量守恒定律,除了镁条在空气中燃烧的实验.(1)请写出镁条与氧气反应的化学方程式2Mg+O2 $\frac{\underline{\;点燃\;}}{\;}$2MgO.
(2)镁条完全燃烧后,小明发现燃烧产物的质量大于反应物镁条的质量,认为这个反应不遵循质量守恒定律,我不同意(“同意”或“不同意”)小明的观点,因为所有的化学反应都遵循质量守恒定律.
(3)小红按如图装置改进实验,验证了质量守恒定律,却发现产物中还有少量黄色固体.
【提出问题】黄色固体是什么呢?
【查阅资料】①通过查阅资料,记录了下列几种物质的颜色:
| 物质 | MgO | MgCl2 | Mg3N2 |
| 颜色 | 白色 | 白色 | 淡黄色 |
【做出猜想】黄色固体是Mg3N2
【实验探究】请你设计实验方案,验证猜想:将镁条放在纯净的氮中点燃,产生黄色固体,证明产物是氮化镁.
【反思与交流】①小华同学认为,在查阅资料时,有一种物质完全可以不用考虑,请推断该物质是氯化镁(填名称),你的理由是空气中不含氯元素;
②写出镁条与氮气反应的化学方程式3Mg+N2$\frac{\underline{\;点燃\;}}{\;}$Mg3N2;
③空气中N2的含量远大于O2的含量,而镁条在空气中燃烧生成MgO却远多于Mg3N2,为什么呢?请给出合理的解释氧气的化学性质比氮气更活泼.
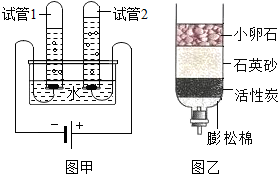 水是生命之源,人类的日常生活与工农业生产都离不开水.
水是生命之源,人类的日常生活与工农业生产都离不开水.