题目内容
现有一包白色粉末可能由NaCl、Na2CO3、Na2SO4、FeCl3、MgCl2
中的一种或几种组成.现做如下实验:
(1)取白色粉末加水溶解得无色透明溶液;
(2)取(1)所得溶液少量加入NaOH溶液看不到明显现象;
(3)另取少量粉末加入稀盐酸,无明显现象.
则:由实验(1)可知原粉末中一定没有 ;
由实验(2)可知原粉末中一定没有 ;
由实验(3)可知原粉末中一定没有 ;
根据上述实验可得出原粉末中可能有的物质是 ;
为确定原粉末是纯净物还是混合物继续做如下实验:
(4)取(1)所得溶液少量,滴加A产生白色沉淀;
(5)继续滴加A至再无白色沉淀生成,静置,取上层清液少许滴加溶液B无明显现象.
则:由实验(4)可知,原粉末中一定有 ;
由实验(5)可知原粉末中一定没有 ;
A、B中溶质的化学式分别是:A B .
中的一种或几种组成.现做如下实验:
(1)取白色粉末加水溶解得无色透明溶液;
(2)取(1)所得溶液少量加入NaOH溶液看不到明显现象;
(3)另取少量粉末加入稀盐酸,无明显现象.
则:由实验(1)可知原粉末中一定没有
由实验(2)可知原粉末中一定没有
由实验(3)可知原粉末中一定没有
根据上述实验可得出原粉末中可能有的物质是
为确定原粉末是纯净物还是混合物继续做如下实验:
(4)取(1)所得溶液少量,滴加A产生白色沉淀;
(5)继续滴加A至再无白色沉淀生成,静置,取上层清液少许滴加溶液B无明显现象.
则:由实验(4)可知,原粉末中一定有
由实验(5)可知原粉末中一定没有
A、B中溶质的化学式分别是:A
考点:物质的鉴别、推断,碱的化学性质,盐的化学性质
专题:混合物组成的推断题
分析:本题属于推断题,根据题目给出的信息:取白色粉末加水溶解得无色透明溶液,因此一定没有氯化铁,因为氯化铁溶于水是黄色溶液;取(1)所得溶液少量加入NaOH溶液看不到明显现象,说明一定没有氯化镁,因为氢氧化镁是白色沉淀;另取少量粉末加入稀盐酸,无明显现象,说明一定没有碳酸钠;检验氯离子与硫酸根离子时,要先检验硫酸根离子,硫酸根离子应该用钡离子检验,取(1)所得溶液少量,滴加A产生白色沉淀,那么A应该是硝酸钡溶液,说明一定有硫酸钠;继续滴加A至再无白色沉淀生成,静置,取上层清液少许滴加溶液B无明显现象,溶液B是硝酸银溶液,因为银离子可以检验氯离子,无明显现象,说明一定没有氯化钠.
解答:解:(1)取白色粉末加水溶解得无色透明溶液,因此一定没有氯化铁,因为氯化铁溶于水是黄色溶液;故答案为:FeCl3;
(2)取(1)所得溶液少量加入NaOH溶液看不到明显现象,说明一定没有氯化镁,因为氢氧化镁是白色沉淀,故答案为:MgCl2;
(3)另取少量粉末加入稀盐酸,无明显现象,说明一定没有碳酸钠;那么NaCl、Na2SO4可能有也可能没有,故答案为:Na2CO3;NaCl、Na2SO4;
(4)检验氯离子与硫酸根离子时,要先检验硫酸根离子,硫酸根离子应该用钡离子检验,取(1)所得溶液少量,滴加A产生白色沉淀,那么A应该是硝酸钡溶液,说明一定有硫酸钠;继续滴加A至再无白色沉淀生成,静置,取上层清液少许滴加溶液B无明显现象,溶液B是硝酸银溶液,因为银离子可以检验氯离子,无明显现象,说明一定没有氯化钠;故答案为:Na2SO4;NaCl
(5)硫酸根离子应该用钡离子检验,取(1)所得溶液少量,滴加A产生白色沉淀,那么A应该是硝酸钡溶液;因为银离子可以检验氯离子,因此溶液B是硝酸银溶液,答案为:Ba(NO3)2;AgNO3;
(2)取(1)所得溶液少量加入NaOH溶液看不到明显现象,说明一定没有氯化镁,因为氢氧化镁是白色沉淀,故答案为:MgCl2;
(3)另取少量粉末加入稀盐酸,无明显现象,说明一定没有碳酸钠;那么NaCl、Na2SO4可能有也可能没有,故答案为:Na2CO3;NaCl、Na2SO4;
(4)检验氯离子与硫酸根离子时,要先检验硫酸根离子,硫酸根离子应该用钡离子检验,取(1)所得溶液少量,滴加A产生白色沉淀,那么A应该是硝酸钡溶液,说明一定有硫酸钠;继续滴加A至再无白色沉淀生成,静置,取上层清液少许滴加溶液B无明显现象,溶液B是硝酸银溶液,因为银离子可以检验氯离子,无明显现象,说明一定没有氯化钠;故答案为:Na2SO4;NaCl
(5)硫酸根离子应该用钡离子检验,取(1)所得溶液少量,滴加A产生白色沉淀,那么A应该是硝酸钡溶液;因为银离子可以检验氯离子,因此溶液B是硝酸银溶液,答案为:Ba(NO3)2;AgNO3;
点评:本考点属于物质的推断题,是通过对实验方法和过程的探究,在比较鉴别的基础上,得出了正确的实验结论.本考点是中考的重要内容之一,一般有两种类型:一是图框式推断题;二是文字描述型推断题;本题属于第二种类型.不论哪一种类型,都是通过实验现象,从而得出物质的组成.此考点主要出现在填空题和实验题中.

练习册系列答案
相关题目
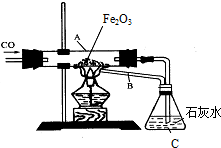 有位同学设计了下列实验(装置及药品如图所示),仔细观察后回答下列问题.
有位同学设计了下列实验(装置及药品如图所示),仔细观察后回答下列问题. 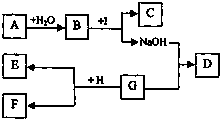 如图中的A-I为九年级化学所学的物质.已知A为金属氧化物,C为大理石的主要成分,D为蓝色沉淀,E为单质,F为浅绿色溶液,F、G、I均为只含有一种溶质的溶液.“→”表示物质间存在着相互转化的关系(部分生成物未标出),如图所示.请回答下列问题:
如图中的A-I为九年级化学所学的物质.已知A为金属氧化物,C为大理石的主要成分,D为蓝色沉淀,E为单质,F为浅绿色溶液,F、G、I均为只含有一种溶质的溶液.“→”表示物质间存在着相互转化的关系(部分生成物未标出),如图所示.请回答下列问题: