题目内容
17.在一定质量的氯化钠溶液中加入硝酸银溶液至氯化钠反应完全,产生的沉淀经过过滤、洗涤、干燥、称量,沉淀质量恰好等于原氯化钠溶液的质量的二分之一.则原氯化钠溶液溶质的质量分数约为( )| A. | 10% | B. | 20% | C. | 30% | D. | 40% |
分析 根据题目给出的信息利用化学方程式可以求出氯化钠与氯化银的质量比,由于沉淀质量恰好等于原氯化钠溶液的质量的二分之一,据此可求出原氯化钠溶液溶质的质量分数约.
解答 解:由方程式AgNO3+NaCl═AgCl↓+NaNO3可知,氯化钠与氯化银的质量比是:58.5:143.5,由于沉淀质量恰好等于原氯化钠溶液的质量的二分之一.则原氯化钠溶液溶质的质量分数约为:$\frac{58.5}{143.5×2}×100%$≈20%,所以B正确.
故选B.
点评 本题主要考查根据化学方程式进行计算的能力,难度不大,解答本题的关键是利用好沉淀质量恰好等于原氯化钠溶液的质量的二分之一个信息.

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目
7.掌握化学知识有助于我们更健康地生活,下列做法正确的是( )
| A. | 随意服用保健品补充各种微量元素 | |
| B. | 霉变的大米用水泡去表面的霉点后食用 | |
| C. | 用甲醛浸泡海鲜产品来延长食品保质期 | |
| D. | 不吃或少吃含亚硝酸盐的熟食制品 |
2.下列铁制品的防锈方法不合理的是( )
| A. | 公交车扶手一涂防锈油 | B. | 水龙头-镀防护金属 | ||
| C. | 汽车外壳一烧漆 | D. | 脸盆一烧涂搪瓷 |
9.在取用药品的实验操作,下列操作正确的是( )
| A. | 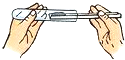 取粉末药品 | B. | 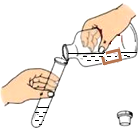 取液体药品 | C. | 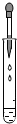 滴加液体 | D. | 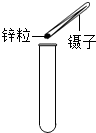 取块状固体 |
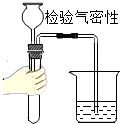

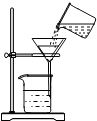
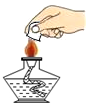
 化学是从微观的角度研究物质的组成、结构及其变化的学科,构成物质的粒子之间关系如图所示.
化学是从微观的角度研究物质的组成、结构及其变化的学科,构成物质的粒子之间关系如图所示.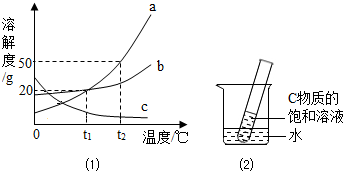 已知a、b、c三种物质的溶解度曲线如图1,根据题意回答下列问题.
已知a、b、c三种物质的溶解度曲线如图1,根据题意回答下列问题.