题目内容
17.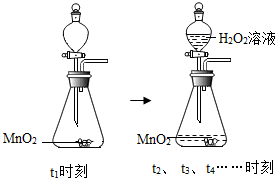 某兴趣小组用如图所示装置测定一瓶久置过氧化氢溶液的溶质质量分数.实验过程中,用电子天平测得不同时刻装置及药品质量随时间变化的数据见表.
某兴趣小组用如图所示装置测定一瓶久置过氧化氢溶液的溶质质量分数.实验过程中,用电子天平测得不同时刻装置及药品质量随时间变化的数据见表. | 实验时间 | t1 | t2 | t3 | t4 | t5 | t6 |
| 关闭活塞 | 打开活塞 | |||||
| 质量/g | 58.6 | 101.1 | 100.8 | 100.5 | 100.3 | 100.3 |
(2)计算这瓶久置过氧化氢溶液的溶质质量分数.
分析 (1)根据质量守恒定律计算生成氧气的质量;
(2)根据化学方程式和生成氧气的质量进行计算.
解答 解:(1)生成氧气的质量为:101.1g-100.3g=0.8g;
(2)参加反应的过氧化氢质量为x
2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑
68 32
x 0.8g
$\frac{68}{x}$$\frac{32}{0.8g}$
x=1.7g
所以这瓶久置过氧化氢溶液的溶质质量分数为:$\frac{1.7g}{101.1g-58.6g}$×100%=4%.
故答案为:(1)0.8;
(2)4%.
点评 本题主要考查学生根据质量守恒定律,运用化学方程式和质量分数公式进行计算的能力.

练习册系列答案
相关题目
7.下列说法中不正确的是( )
| A. | 把铅加入锡中制成合金焊锡,主要目的是降低焊锡的熔点 | |
| B. | 衣料中的棉、羊毛等都属于合成有机高分子材料 | |
| C. | 活性炭能净化水是因为有吸附作用 | |
| D. | 洗涤剂能清洗油污,因为它有乳化作用 |
8.下列物质既是空气的成分,又属于氧化物的是( )
| A. | 氧气 | B. | 二氧化碳 | C. | 碳酸 | D. | 氩气 |
12.良好的环境和充足的资源是人类赖以生存的两个方面,下列叙述中正确的是( )
| A. | “白色污染”的产生与纸张的随意丢弃有关 | |
| B. | 城市中“光污染”现象是由光的漫反射造成的 | |
| C. | “水华”是水体富营养化的结果,所以农业上要合理使用化肥 | |
| D. | 石油被称为“工业的血液”所以应加速石油开采,以提高人类的生活质量 |
7.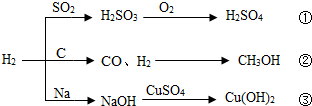 如图为与水相关的部分转化关系(水作反应物或生成物,部分产物和反应条件未列出).下列说法错误的是( )
如图为与水相关的部分转化关系(水作反应物或生成物,部分产物和反应条件未列出).下列说法错误的是( )
 如图为与水相关的部分转化关系(水作反应物或生成物,部分产物和反应条件未列出).下列说法错误的是( )
如图为与水相关的部分转化关系(水作反应物或生成物,部分产物和反应条件未列出).下列说法错误的是( )| A. | 图中所示的反应中均有元素化合价的改变 | |
| B. | 途径①是硫酸型酸雨形成的重要途径 | |
| C. | 工业上可用途径②制取有机物,当合成甲醇CH3OH时,CO、H2投料质量比为14:1 | |
| D. | 把金属钠投入到硫酸铜溶液中,发生途径③反应,反应不生成铜单质 |
 合理膳食、安全饮食是健康的保障.
合理膳食、安全饮食是健康的保障.