题目内容
实验室用H2还原Fe2O3,当a g Fe2O3部分变黑时,即停止加热,待冷却后称得固体质量为b g,水(假设未损失)为c g,实验过程中共用去d g H2,则被还原的Fe2O3的质量为多少g?
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:析题意知,氢气还原氧化铁实验中停止加热时,防止生成的铁被氧化,要继续通入氢气直至冷却,可知用去氢气dg并未全部参加还原氧化铜的反应,所以,在根据化学方程式进行计算时,不能使用氢气质量进行计算;反应前后固体质量差为氧化铁在反应中失去氧元素的质量,失去的氧元素与氢化合成水,因此,由氧元素质量可计算被还原的Fe2O3的质量.
解答:解:反应中氧化铁失去O元素的质量=ag-bg=(a-b)g;
则被还原的Fe2O3的质量为
g=
g
答案:被还原的Fe2O3的质量为
g
则被还原的Fe2O3的质量为
| a-b | ||
|
| 10(a-b) |
| 3 |
答案:被还原的Fe2O3的质量为
| 10(a-b) |
| 3 |
点评:根据化学方程式进行计算时,所使用的物质的质量必须为完全反应时物质的质量,未参加反应的物质的质量不能代入化学方程式进行计算.

练习册系列答案
相关题目
由Na2CO3和CaCO3组成的混合物中,经测定其中碳元素的质量分数为11.65%,则在以下这六个量中:①Na元素的质量分数;②Ca元素的质量分数;③氧元素的质量分数;④CaCO3的质量分数;⑤Na2CO3的质量分数;⑥Na2CO3和CaCO3的质量比.能确定的是( )
| A、都不能确定 |
| B、只有③能确定 |
| C、只有④⑤⑥能确定 |
| D、都能确定 |
下列各种纤维中的主要成份属于有机合成材料的是( )
| A、涤纶 | B、蚕丝 | C、麻 | D、棉花 |

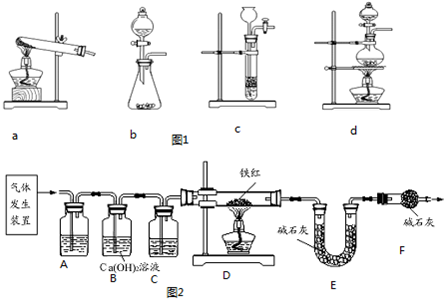
 某校化学兴趣小组的同学们就空气中氧气的含量进行如图所示的实验探讨:
某校化学兴趣小组的同学们就空气中氧气的含量进行如图所示的实验探讨: