题目内容
4.乙醇(C2H5OH)是以高粱、玉米、薯类等为原料,经过发酵、蒸馏制得,属于可再生资源.乙醇在足量的氧气中完全燃烧时生成二氧化碳和水,如果氧气不足,乙醇燃烧可能还有一氧化碳生成.现用下图实验装置进行实验,检验乙醇的燃烧产物中是否有二氧化碳和一氧化碳: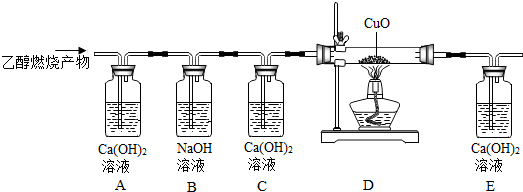
请回答下列问题:
(1)写出乙醇在足量的氧气中完全燃烧的化学方程式C2H5OH+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O.
(2)有甲、乙、丙三个同学分别完成上述实验并将观察到的现象填写在下表中,试用“有”、“没有”和“可能有”填写下表中的实验结论.
| 实验现象 | 实验结论 | ||||
| A装置 | C装置 | E装置 | 是否有二氧化碳 | 是否有一氧化碳 | |
| 甲同学 | 石灰水变浑浊 | 石灰水没变浑浊 | 石灰水没变浑浊 | 有 | |
| 乙同学 | 石灰水变浑浊 | 石灰水变浑浊 | 石灰水变浑浊 | ||
| 丙同学 | 石灰水没变浑浊 | 石灰水没变浑浊 | 石灰水变浑浊 | 有 | |
分析 (1)根据乙醇燃烧生成二氧化碳和水,写出反应的化学方程式即可.
(2)装置A用于检验乙醇燃烧是否生成二氧化碳;装置B则用于吸收二氧化碳;装置C用于检验二氧化碳是否已完全吸收;装置D用于把一氧化碳气体转变为二氧化碳;装置E检验装置D排出气体中是否含有二氧化碳;根据以上装置作用的分析,由实验现象判断乙醇燃烧的生成物;
(3)根据化学变化前后元素种类和质量不变,乙醇燃烧生成物二氧化碳、一氧化碳中碳元素质量总和即乙醇中碳元素质量,由乙醇中C、H元素质量比计算出H元素质量,由H元素质量计算生成水的质量.
解答 解;(1)乙醇燃烧生成二氧化碳和水,反应的化学方程式为:C2H5OH+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O.
故答案为:(1)C2H5OH+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O;
(2)装置A中石灰水变浑浊,可以说明燃烧生成二氧化碳;
装置C中石灰水不浑浊,说明混合气体中二氧化碳已完全吸收,变浑浊则说明前面生成的二氧化碳没有吸收完全,对后面二氧化碳的判断带来影响;
装置E中石灰水变浑浊,说明气体中有二氧化碳;
故答案为:
| 实验现象 | 实验结论 | ||||
| A装置 | C装置 | E装置 | 是否有二氧化碳 | 是否有一氧化碳 | |
| 甲同学 | 没有 | ||||
| 乙同学 | 有 | 可能有 | |||
| 丙同学 | 没有 | ||||
5.6g一氧化碳中C元素质量=5.6g×$\frac{12}{28}$×100%=2.4g
则燃烧的乙醇中C元素质量=1.2g+2.4g=3.6g
乙醇中C、H元素质量比=24:6=4:1,则乙醇中H元素质量=$\frac{3.6g}{4}$=0.9g
乙醇燃烧生成水的质量=0.9g÷$\frac{2}{18}$×100%=8.1g
故答案为:8.1g.
点评 可燃物在氧气充足时完全燃烧,其中C元素生成二氧化碳、H元素生成水;在氧气不足时不完全燃烧,可燃物中的C元素就可能生成二氧化碳或一氧化碳.

练习册系列答案
 字词句段篇系列答案
字词句段篇系列答案
相关题目
14.炒菜时,油锅里的油着火了,应采取的最适宜的灭火措施是下列的( )
| A. | 向油锅里倒水 | B. | 向油锅里撒沙子 | ||
| C. | 把油锅端下来 | D. | 盖上锅盖并把油锅远离火源 |
15.下列物质的用途不是利用其化学性质的是( )
| A. | 氧气用于高炉炼钢 | B. | 液态氮做制冷剂 | ||
| C. | 氢气做清洁高效的新能源 | D. | 稀有气体用做保护气 |
9.下列化学用语与含义相符的是( )
| A. | Mg+2--镁离子 | |
| B. | $\stackrel{+2}{Ca}$O--氧化钙中钙元素的化合价为+2价 | |
| C. | 2H--2个氢元素 | |
| D. | O2--2个氧原子 |
13. 如图是测定空气中氧气含量的实验装置.下列有关该实验的说法正确的是( )
如图是测定空气中氧气含量的实验装置.下列有关该实验的说法正确的是( )
 如图是测定空气中氧气含量的实验装置.下列有关该实验的说法正确的是( )
如图是测定空气中氧气含量的实验装置.下列有关该实验的说法正确的是( )| A. | 使用红磷的量越多,最终进入集气瓶的水也越多 | |
| B. | 若实验过程中没有夹紧止水夹或燃烧匙插入集气瓶的速度太慢,都会影响测定的结果 | |
| C. | 本实验可以证明空气含有N2、O2、CO2和稀有气体 | |
| D. | 燃烧匙中的红磷可以换成硫或木炭 |
14.鉴别下列各组物质,括号中选用的方法或试剂,不合理的是( )
| A. | 澄清石灰水和烧碱溶液(稀盐酸) | |
| B. | 硫酸铜溶液和高锰酸钾溶液(观察颜色) | |
| C. | 乙醇和食盐水(闻气味) | |
| D. | 纯碱溶液和稀硫酸(酚酞试液) |

