题目内容
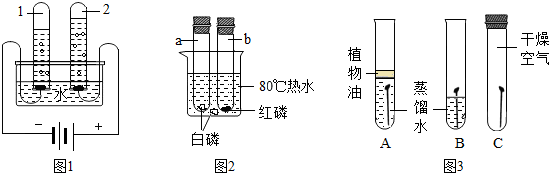
 往如图所示的烧杯中加入一种物质,搅拌后,发现塑料片滑落,加入的物质不可能是( )
往如图所示的烧杯中加入一种物质,搅拌后,发现塑料片滑落,加入的物质不可能是( )| A、浓硫酸 | B、硝酸铵 |
| C、生石灰 | D、氢氧化钠固体 |
考点:溶解时的吸热或放热现象,生石灰的性质与用途
专题:溶液、浊液与溶解度
分析:根据有的物质溶于水时会放出热量,使溶液温度升高,如浓硫酸、氢氧化钠固体等;有的物质与水反应会放出热量,使液体温度升高;如生石灰;也有些物质溶于水时会吸收热量,使溶液温度降低,如硝酸铵等.放出热量会使石蜡熔化,粘在烧杯上的塑料片脱落;溶于水时吸收热量的,石蜡仍为固态,粘在烧杯上的塑料片不会脱落进行解答.
解答:解:A、浓硫酸溶于水时会放出热量,会使石蜡熔化,粘在烧杯上的塑料片脱落;
B、烧杯中加入硝酸铵晶体,溶于水时吸收热量,使溶液的温度下降,所以石蜡仍为固态,粘在烧杯上的塑料片不会脱落;
C、生石灰放入水中与水反应放出热量,会使石蜡熔化,粘在烧杯上的塑料片脱落;
D、氢氧化钠溶于水时会放出热量,会使石蜡熔化,粘在烧杯上的塑料片脱落.
故选B.
B、烧杯中加入硝酸铵晶体,溶于水时吸收热量,使溶液的温度下降,所以石蜡仍为固态,粘在烧杯上的塑料片不会脱落;
C、生石灰放入水中与水反应放出热量,会使石蜡熔化,粘在烧杯上的塑料片脱落;
D、氢氧化钠溶于水时会放出热量,会使石蜡熔化,粘在烧杯上的塑料片脱落.
故选B.
点评:物质溶解于水时有三种表现:溶解时放出热量使溶液温度升高,以氢氧化钠、浓硫酸为代表;溶解时吸收热量使溶液温度降低,以硝酸铵为代表;其它大部分物质溶解时无明显的热量变化,溶液温度基本保持不变.

练习册系列答案
相关题目
下列粒子结构示意图中表示阴离子的是( )
A、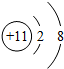 |
B、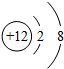 |
C、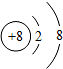 |
D、 |
下表是NaCl、KNO3 在不同温度时的溶解度
据此数据,判断下列说法错误的是( )
| 温度 | 10 | 20 | 30 | 40 | 50 | 60 | |
| 溶解度/g | NaCl | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
| KNO3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | |
| A、KNO3 和NaCl 的溶解度曲线在20℃~30℃温度范围内会相交 |
| B、在60℃时,KNO3 的饱和溶液105g加入95g水后,溶液中溶质的质量分数为27.5% |
| C、在20℃时,NaCl 和KNO3 固体各35g分别加入两只各盛有100g水的烧杯中,均不能形成饱和溶液 |
| D、从含有少量NaCl 的KNO3 饱和溶液中得到较多的KNO3 晶体,通常采用冷却热的饱和溶液法 |
造成酸雨的主要物质是( )
| A、甲烷和一氧化碳 |
| B、二氧化硫和一氧化碳 |
| C、一氧化碳和二氧化碳 |
| D、二氧化硫和二氧化氮 |
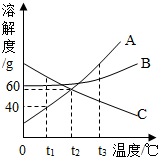 如图为A、B、C三种固体物质的溶解度曲线,请回答下列问题:
如图为A、B、C三种固体物质的溶解度曲线,请回答下列问题: