题目内容
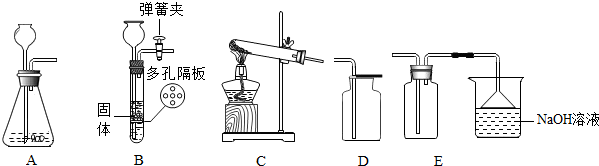
16. 如图是A、B、C三种物质的溶解度曲线,据图回答:
如图是A、B、C三种物质的溶解度曲线,据图回答:(1)t2℃时30gA物质加入到50g水中不断搅拌,能形成溶液的质量为75g.
(2)A、B、C三种物质分别与少量氯化钠形成混合物,其中最适合使用的冷却热饱和溶液的方法除去氯化钠杂质的是A(填写序号).
(3)将t1℃时A、B、C三种物质饱和溶液的温度升高到t2℃时,三种溶液的溶质质量分数由大小关系是B>A>C.
(4)在t2℃下,将C物质的不饱和溶液变为饱和溶液,下列有关说法不正确的是B.
A.溶剂的质量可能变小 B.溶质的质量一定不变
C.溶液的质量可能变大 D.溶质的质量分数一定变大.
分析 根据物质的溶解度曲线、溶质质量、溶剂质量可以判断配制的溶液质量;
一种物质的溶解度受温度变化影响较大,一种物质的溶解度受温度变化影响较小,可以用降温结晶的方法分离;
根据物质的溶解度曲线可以判断随着温度的变化,溶质质量分数变化的情况;
饱和溶液和不饱和溶液之间可以相互转化.
解答 解:(1)t2℃时,A的溶解度是50g,30gA物质加入到50g水中不断搅拌,只能够溶解25g,能形成溶液的质量为:25g+50g=75g;
(2)A和B的溶解度随着温度的升高而增大,并且A的溶解度受温度变化影响较大,因此A、B、C三种物质分别与少量氯化钠形成混合物,其中最适合使用的冷却热饱和溶液的方法除去氯化钠杂质的是A;
(3)t1℃时,B的溶质质量分数最大,A和C的质量分数相等,将t1℃时A、B、C三种物质饱和溶液的温度升高到t2℃时,A和B变成不饱和溶液,溶质质量分数不变,C仍然是饱和溶液,但是溶解度减小,溶质质量分数变小,因此三种溶液的溶质质量分数由大小关系是B>A>C;
(4)A.溶剂的质量可能变小,因为恒温蒸发溶剂可以使不饱和溶液变成饱和溶液,该选项说法正确;
B.溶质的质量可以增大,因为加入溶质也可以使不饱和溶液变成饱和溶液,该选项说法不正确;
C.溶液的质量可能变大,因为加入溶质时容易质量增大,该选项说法正确;
D.溶质的质量分数一定变大,因为无论是恒温蒸发溶剂,还是加入溶质,都能够使溶质质量分数增大,该选项说法正确.
故填:75g;A;B>A>C;B.
点评 溶解度曲线能定量地表示出溶解度变化的规律,从溶解度曲线可以看出:同一溶质在不同温度下的溶解度不同;同一温度下,不同溶质的溶解度可能相同,也可能不同;温度对不同物质的溶解度影响不同.

练习册系列答案
相关题目
11.用分子、原子的相关知识解释下列现象,正确的是( )
| A. | 一块金属很难被压缩,说明原子之间没有间隔 | |
| B. | 湿衣服晾在太阳下干的快,说明分子运动速率与温度有关 | |
| C. | 将二氧化碳气体制成干冰,体积变小是由于分子体积变小 | |
| D. | 分离液态空气制氧气说明分子可以再分 |
1.古语道:“人要实,火要虚”.意思是说:“做人要脚踏实地,事业才能有成;燃烧要架空,火才能更旺”.从燃烧的条件看,“火要虚”的实质是( )
| A. | 提高可燃物的着火点 | B. | 增大可燃物的热值 | ||
| C. | 增大可燃物与空气的接触面积 | D. | 提高空气中氧气的含量 |
6.在NF3中,F元素化合价为-1价,则N元素化合价为( )
| A. | +3 | B. | 0 | C. | +1 | D. | -3 |
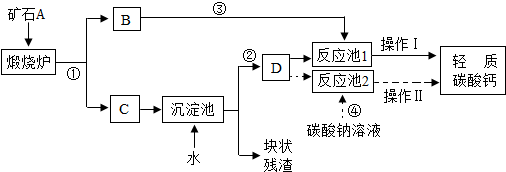
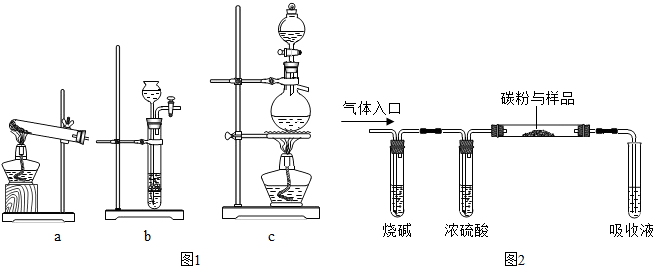
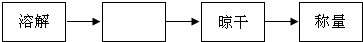
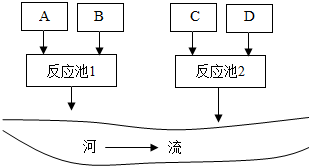 某化学试剂厂A,B,C,D四个车间排放的废水中,分别含有氢氧化钠、硫酸铜、碳酸钠、硫酸中的一种,在不加其他试剂的情况下,若控制流量,将它们排放到反应池中,使其恰好完全反应,最后可形成不污染环境的废液排入河流.如图所示:
某化学试剂厂A,B,C,D四个车间排放的废水中,分别含有氢氧化钠、硫酸铜、碳酸钠、硫酸中的一种,在不加其他试剂的情况下,若控制流量,将它们排放到反应池中,使其恰好完全反应,最后可形成不污染环境的废液排入河流.如图所示: