题目内容
19.化学小组同学在课外读物中看到“Na2O2广泛应用于潜艇的呼吸供氧和CO2的去除”他们决定验证CO2与Na2O2反应的反应及其产物.他们查阅资料知道:①Na2O2是一种淡黄色固体,常温下与CO2、H2O等物质反应,反应的化学方程式分别为:2Na2O2+2CO2═2Na2CO3+O2、2Na2O2+2H2O═4NaOH+O2↑.
②CO2既不与NaHCO3反应,也不溶于饱和的NaHCO3溶液中.
③Na2O2与稀盐酸反应时,生成NaCl、H2O和O2.
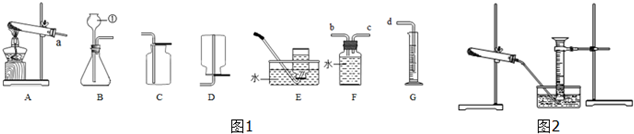
他们在老师的指导下用稀盐酸和石灰石反应,利用如图所示装置(部分夹持仪器已略去)进行实验.

(1)NaHCO3能与盐酸发生复分解反应,化学方程式为NaHCO3+HCl=NaCl+H2O+CO2↑;
(2)为验证CO2与Na202反应有氧气生成,实验时需将上述仪器正确连接,其导管的 连接顺序从左到右依次为:m→e,f接a,b接g,h接c(填导管的字母);
(3)检验有无Na2CO3生成的方法是取E中反应后的固体放于试管,滴加稀盐酸,将生成的气体通入澄清的石灰水,澄清的石灰水变浑浊;
(4)本实验中需要使用D装置,其目的是除去二氧化碳气体中的HCl.
分析 (1)根据化学方程式的书写方法来分析;
(2)分析装置的作用,A是制取二氧化碳,B是干燥二氧化碳,C是除去未反应的二氧化碳,D是除去氯化氢气体,E是二氧化碳与过氧化钠反应,然后结合题意:检验反应产物,确定装置的连接顺序,洗气装置导管是长进短出;
(3)依据碳酸钠可用稀盐酸检验是否生成二氧化碳进行分析;
(4)根据碳酸氢钠可与氯化氢气体反应来分析.
解答 解:(1)碳酸氢钠与稀盐酸反应生成氯化钠、水和二氧化碳,故填:NaHCO3+HCl=NaCl+H2O+CO2↑;
(2)根据题意,Na2O2是一种淡黄色固体,常温下与CO2、H2O等物质反应,Na2O2与稀盐酸可反应,生成NaCl、H2O和O2,CO2既不与NaHCO3反应,也不溶于饱和的NaHCO3溶液中;所以要让二氧化碳与过氧化钠反应,先要排除可能稀盐酸挥发的氯化氢气体,将生成的二氧化碳通过D,由于气体从溶液中出来时要带来水蒸气,故要通过浓硫酸除去水蒸气,然后将除杂后的二氧化碳通入过氧化钠,通过氢氧化钠溶液除去未反应的二氧化碳,最后检验生成的气体是否是氧气;故填:e,f接a,b接g,h接c;
(3)检验有Na2CO3生成的方法是:取E中反应后的固体放于试管,滴加稀盐酸,将生成的气体通入澄清的石灰水,若澄清的石灰水变浑浊,说明有碳酸钠生成;故填:取E中反应后的固体放于试管,滴加稀盐酸,将生成的气体通入澄清的石灰水,澄清的石灰水变浑浊;
(4)使气体通过D装置的原因是除去二氧化碳中氯化氢气体,防止进入E装置与过氧化钠固体反应造成干扰;故填:二氧化碳.
点评 分析装置的作用,能正确分析题目所蕴含的信息,并能依据题意分析解答相关问题是解题的关键.

练习册系列答案
 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目
10.小亮在实验室发现一瓶盛有无色溶液的试剂瓶,其标签破损,从残余部分只能看出溶质质量分数为10%,具体是什么物质无法辨认.老师告诉他,这瓶溶液可能是氢氧化钠、氯化钠、氢氧化钙或是碳酸钠中的一种.
(1)小亮查阅资料后,认为该溶液不可能是氢氧化钙溶液
(2)小亮取少量样品于试管中,滴加酚酞试液,试液变红,该溶液不可能是NaCl(化学式)
(3)为了确定该溶液的成分,小亮同学继续进行如下实验,请一起参与,并填写下列实验报告.
(1)小亮查阅资料后,认为该溶液不可能是氢氧化钙溶液
(2)小亮取少量样品于试管中,滴加酚酞试液,试液变红,该溶液不可能是NaCl(化学式)
(3)为了确定该溶液的成分,小亮同学继续进行如下实验,请一起参与,并填写下列实验报告.
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量溶液于试管,滴加氯化钙溶液. | 该溶液是碳酸钠溶液.有关反应的化学方程式为:Na2CO3+CaCl2═CaCO3↓+2NaCl. |
8.下列实验设计能达到实验目的是( )
| 选项 | A | B | C | D |
| 实验设计 |  | 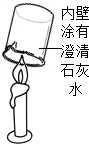 |  | 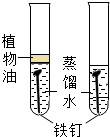 |
| 实验目的 | 证明二氧化碳与水反应生成碳酸 | 证明石蜡成分中含有碳元素 | 探究可燃物燃烧需要氧气和温度达到着火点 | 证明铁生锈是水和氧气共同作用的结果 |
| A. | A | B. | B | C. | C | D. | D |
5.下列涉及“水”的实验中,操作方法正确的是( )
| A. | 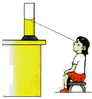 读取量筒中水的体积 | |
| B. |  使刚停止沸腾的水向外抽气 重新沸腾 | |
| C. |  结晶时待水完全蒸发,先熄灭酒精灯后再停止加热 | |
| D. |  氧气收集完毕,将导管移出水面 |
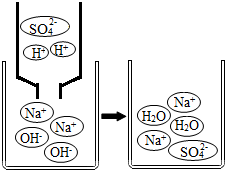 在1支盛有3毫升氢氧化钠稀溶液的试管里,滴加1滴酚酞试液,再向试管里逐滴加入稀硫酸,边滴边振荡,直到红色刚好褪去.
在1支盛有3毫升氢氧化钠稀溶液的试管里,滴加1滴酚酞试液,再向试管里逐滴加入稀硫酸,边滴边振荡,直到红色刚好褪去. 已知氢氧化铝是一种不溶于水的白色沉淀,能与稀盐酸反应,也能与过量的氢氧化钠溶液反应,氢氧化铝与氢氧化钠溶液反应的化学方程式为:Al(OH)3+NaOH═NaAlO2+2H2O.生成的偏酸钠(NaAlO3)可溶于水(但Mg(OH)2固体不溶于NaOH溶液.现有含AlCl3和MgCl2的混合溶液50g,向溶液中逐滴加入溶质质量分数为10%的NaOH溶液,生成沉淀质量与加入NaOH溶液质量关系如图所示:
已知氢氧化铝是一种不溶于水的白色沉淀,能与稀盐酸反应,也能与过量的氢氧化钠溶液反应,氢氧化铝与氢氧化钠溶液反应的化学方程式为:Al(OH)3+NaOH═NaAlO2+2H2O.生成的偏酸钠(NaAlO3)可溶于水(但Mg(OH)2固体不溶于NaOH溶液.现有含AlCl3和MgCl2的混合溶液50g,向溶液中逐滴加入溶质质量分数为10%的NaOH溶液,生成沉淀质量与加入NaOH溶液质量关系如图所示: