题目内容
8.下列化学反应既不是化合反应,又不是分解反应但属于氧化反应的是( )| A. | 铁在氧气中燃烧 | B. | 过氧化氢与二氧化锰制氧气 | ||
| C. | 水的电解 | D. | 石蜡在氧气中燃烧 |
分析 化合反应:两种或两种以上物质反应后生成一种物质的反应,其特点可总结为“多变一”;分解反应:一种物质反应后生成两种或两种以上的物质,其特点可总结为“一变多”;物质与氧发生的化学反应是氧化反应;据此进行分析判断.
解答 解:A、铁在氧气中燃烧生成四氧化三铁,该反应符合“多变一”的特征,属于化合反应,故选项错误.
B、过氧化氢在二氧化锰的催化作用下生成水和氧气,该反应符合“一变多”的特征,属于分解反应,故选项错误.
C、水通电分解生成氢气和氧气,该反应符合“一变多”的特征,属于分解反应,故选项错误.
D、石蜡在氧气中燃烧生成二氧化碳和水,该反应的生成物是两种,不符合“多变一”的特征;该反应的反应物是两种,不符合“一变多”的特征;既不是化合反应,又不是分解反应;但该反应是物质与氧气发生的反应,属于氧化反应;故选项正确.
故选:D.
点评 本题难度不大,掌握化合反应的特征(“多变一”)、分解反应的特征(“一变多”)、氧化反应的特征是正确解答本题的关键.

练习册系列答案
相关题目
18.下列区分物质的方法不正确的是( )
| A. | 硬水和软水-加肥皂水 | |
| B. | 氢氧化钠溶液、碳酸钠溶液-加入酚酞试液 | |
| C. | 氧气、二氧化碳-插入带火星的木条 | |
| D. | 硝酸铵固体、氢氧化钠固体-加水 |
19.有人用下列方法除去硬水中某些可溶性钙、镁化合物,以降低水的硬度,你认为可行的方法是( )
| A. | 煮沸 | B. | 静置 | C. | 过滤 | D. | 加明矾 |
16.分子、原子和离子都是构成物质的基本粒子.下列物质由离子构成的是( )
| A. | 氯化钠 | B. | 蒸馏水 | C. | 氮气 | D. | 铁 |
3.利用如图装置进行实验.实验前K1、K2、K3均已关闭.
(1)检查装置气密性:保持K1关闭,打开K2、K3,向B中加水至液面浸没下端导管口,用手捂住A瓶外壁,说明装置的左侧气密性良好的现象是看到B装置左侧导管口有气泡冒出;用同样原理可以检查装置另一侧的气密性.
(2)实验1中,气体收集完毕后,在不拆卸装置的情况下,使A中未反应的过氧化氢溶液大部分转移到B中的操作是打开k2,k3,关闭k1.
(3)实验2中,打开K2和K3后所观察到的现象是澄清石灰水变浑浊,A中发生反应的化学方程式为CO2+Ca(OH)2═CaCO3↓+H2O;当B中液面不再变化时,测得B中减少了160mL水,则A中CO2的体积分数约为50%.
| 装置 内容 | 【实验1】制备气体 | 【实验2】测定气体含量 |
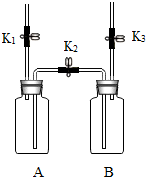 | Ⅰ.打开K1,用注射器向盛有二氧化锰的A中注入过氧化氢溶液,直至液面浸没下端导管口 Ⅱ.在K1上方导管口收集气体 | Ⅰ.A(容积350mL)中为用排空气法收集的CO2,B中装满澄清石灰水.用注射器向A中注入15mL 澄清石灰水(足量,完全吸收CO2),充分反应. Ⅱ.打开K2和K3 |
(2)实验1中,气体收集完毕后,在不拆卸装置的情况下,使A中未反应的过氧化氢溶液大部分转移到B中的操作是打开k2,k3,关闭k1.
(3)实验2中,打开K2和K3后所观察到的现象是澄清石灰水变浑浊,A中发生反应的化学方程式为CO2+Ca(OH)2═CaCO3↓+H2O;当B中液面不再变化时,测得B中减少了160mL水,则A中CO2的体积分数约为50%.
13.下列能量的转化过程中,由化学能转化为电能的是( )
| A. |  蓄电池放电 | B. |  风力发电 | C. |  水力发电 | D. |  太阳能发电 |
6.守恒思想是以定量的角度观察化学世界的永恒主题.
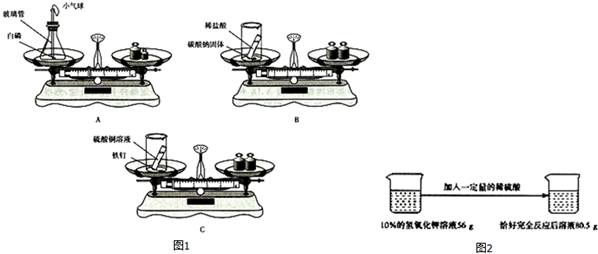
(1)用如图1所示的3个实验验证质量守恒定律,其中实验后天平不能保持平衡的是B(填序号),理由是装置未密闭,生成的二氧化碳气体逸出,导致左盘中容器内的物质总质量减少.
(2)卫星运载火箭的动力由高氯酸铵(NH4ClO4)发生反应提供,化学方程式为:
2NH4ClO4$\frac{\underline{\;高温\;}}{\;}$N2↑+C12↑+202↑+4X.则
①X的化学式为H2O.
②该反应属于基本反应类型中的分解反应.
(3)从微观角度分析有助于我们理解质量守恒定律.在一密闭容器内有四种物质A、B、C、D,它们在一定条件下发生化学反应.经过一段时间后停止反应,其中A、B、C、D的微观示意图和反应前后各物质的质量如下表所示.
①从微观角度分析,化学反应中质量守恒的原因是化学反应前后原子的种类不变,原子的数目不变,原子的质量不变.
②该反应中B和C的质量比为10:9.
③表中x的值是18.
(4)将0.8g草酸亚铁(FeC204)放在一个可称量的敞口容器中加热灼烧,固体质量随温度升高而变化的数据如下(下表中所注明的各温度下,容器中的固体均为纯净物):
①400℃时,容器中的固体为FeO(填化学式).
②400℃~500℃,发生了化合反应(填“分解反应”或“化合反应”).
③600℃~900℃,发生的反应可表示为6Fe2O3$\frac{\underline{\;高温\;}}{\;}$4Fe3O4+O2↑.
(5)根据图2的信息计算:
①加人的稀硫酸质量为24.5g.
②所用稀硫酸溶质的质量分数为20%.(化学方程式:2K0H+H2S04=K2S04+2H20)

(1)用如图1所示的3个实验验证质量守恒定律,其中实验后天平不能保持平衡的是B(填序号),理由是装置未密闭,生成的二氧化碳气体逸出,导致左盘中容器内的物质总质量减少.
(2)卫星运载火箭的动力由高氯酸铵(NH4ClO4)发生反应提供,化学方程式为:
2NH4ClO4$\frac{\underline{\;高温\;}}{\;}$N2↑+C12↑+202↑+4X.则
①X的化学式为H2O.
②该反应属于基本反应类型中的分解反应.
(3)从微观角度分析有助于我们理解质量守恒定律.在一密闭容器内有四种物质A、B、C、D,它们在一定条件下发生化学反应.经过一段时间后停止反应,其中A、B、C、D的微观示意图和反应前后各物质的质量如下表所示.
| 物质 | A | B | C | D |  氮原子 氮原子 氧原子 氧原子 氢原子 氢原子 |
| 微观示意图 |  |  |  | 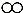 | |
| 反应前质量/g | 100 | 20 | X | y | |
| 反应后质量/g | 32 | 140 | 126 | 46 |
②该反应中B和C的质量比为10:9.
③表中x的值是18.
(4)将0.8g草酸亚铁(FeC204)放在一个可称量的敞口容器中加热灼烧,固体质量随温度升高而变化的数据如下(下表中所注明的各温度下,容器中的固体均为纯净物):
| 温度(℃) | 25 | 350 | 400 | 500 | 600 | 900 |
| 固体质量(g) | 0.80 | 0.80 | 0.40 | 0.44 | 0.44 | 0.43 |
②400℃~500℃,发生了化合反应(填“分解反应”或“化合反应”).
③600℃~900℃,发生的反应可表示为6Fe2O3$\frac{\underline{\;高温\;}}{\;}$4Fe3O4+O2↑.
(5)根据图2的信息计算:
①加人的稀硫酸质量为24.5g.
②所用稀硫酸溶质的质量分数为20%.(化学方程式:2K0H+H2S04=K2S04+2H20)
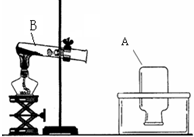 绘制实验装置图是我们初中生应该掌握的一项技能.图是某同学正在绘制的实验室用高锰酸钾制取氧气的装置图.请按要求回答下列问题.
绘制实验装置图是我们初中生应该掌握的一项技能.图是某同学正在绘制的实验室用高锰酸钾制取氧气的装置图.请按要求回答下列问题.