题目内容
水和溶液在生产生活中起着重要的作用。
(1)氢气燃烧是人们认识水组成的开始,该反应的化学方程式为 。
(2)下列实验中,水用来隔绝空气的是 (填字母序号)。
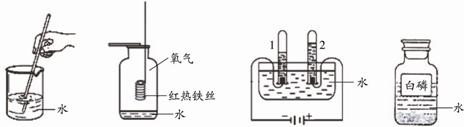 |
A.溶解物质 B.铁丝燃烧 C.水的电解 D.保存白磷
(3)为检测饮用水是否为硬水,可向所取水样及另一软水中加入等量的 来判断。生活中将硬水软化的方法是 ,此过程产生水垢,其成分是CaCO3和Mg(OH)2。实验室从该水垢中提取氯化钙晶体的主要流程如下:
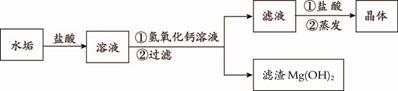 |
向滤液中加入盐酸的目的是 (用化学方程式解释)。
(4)20 ℃时,取甲、乙、丙、丁四种物质各20 g,分别加入到四个盛有50 g水的烧杯中,
充分溶解,情况如下表(温度保持20 ℃),下列说法正确的是 (填字母序号)。
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 未溶解固体的质量 /g | 4.2 | 2 | 0 | 9.2 |
A.所得溶液一定都是饱和溶液
B.溶质质量分数最大的是丙溶液
C.所得四种溶液的质量关系为:丙>乙>甲>丁
D.20 ℃时四种物质溶解度的关系为:丙>乙>甲>丁
(1)2H2 + O2点燃2H2O (2)D
(3)肥皂水 煮沸 Ca(OH)2 + 2HCl = CaCl2 + 2H2O
(4)BCD

 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案 许多植物的花瓣或果实中含有色素,现提取几种植物的花瓣或果实的汁液 ,用稀酸、稀碱和水逐一检验,现象记录如下表:
,用稀酸、稀碱和水逐一检验,现象记录如下表:
| 植物的汁液 | 在酸性溶液中 | 在水中 | 在碱性溶液中 |
| 牵牛花 | 红色 | 紫色 | 蓝色 |
| 万寿菊 | 黄色 | 黄色 | 黄色 |
| 胡萝卜 | 橙色 | 橙色 | 橙色 |
| 玫瑰 | 浅红色 | 浅红色 | 绿色 |
(1)上述植物 的汁液不能用来区别稀硫酸和石灰水的是 、
的汁液不能用来区别稀硫酸和石灰水的是 、 。(填植物的名称)
。(填植物的名称)
(2)手工制作一朵纸玫瑰花,用白醋浸泡后晾干,将所提取的玫瑰汁液均匀喷洒在纸玫瑰上,纸花会变成 。
(3)小亮用此牵牛花汁检测附近造纸厂排放的废液酸碱性,溶液呈蓝色,这次废液显 。
(4)与实验室常用的指示剂石蕊的变色原理相似的是 。(填植物的 名称)
名称)

 石的货车,在高速路上发生意外,燃起大火并伴有大量黑烟,这辆货车在雨中燃烧了很长时间。某化学小组对电石中碳化钙(CaC2)的性质产生了兴趣,进行了下列探究活动。
石的货车,在高速路上发生意外,燃起大火并伴有大量黑烟,这辆货车在雨中燃烧了很长时间。某化学小组对电石中碳化钙(CaC2)的性质产生了兴趣,进行了下列探究活动。 。
。 是在汽油中加入适量的乙醇混合而成的一种燃料。下列叙述正确的是( )A.乙醇汽油是一种新型化合物 B.用玉米、高粱发酵可以制得乙醇汽油
是在汽油中加入适量的乙醇混合而成的一种燃料。下列叙述正确的是( )A.乙醇汽油是一种新型化合物 B.用玉米、高粱发酵可以制得乙醇汽油 D.汽车使用乙醇汽油能减少有害气体排放
D.汽车使用乙醇汽油能减少有害气体排放