题目内容
20.在2Na+2H2O═2NaOH+H2↑中,被氧化的物质是Na.分析 在氧化还原反应中,化合价升高的物质是还原剂,被氧化,发生了氧化反应;化合价降低的物质是氧化剂,被还原,发生了还原反应;据此结合反应的化学方程式、各物质化合价的变化进行分析解答.
解答 解:在2Na+2H2O═2NaOH+H2↑中,Na属于单质,钠元素的化合价为0;氢氧化钠中氢氧根的化合价为-1价,则钠元素显+1价;Na元素的化合价由0价变为+1价,化合价升高,Na是还原剂,被氧化,发生了氧化反应.
水中氢元素显+1价;氢气属于单质,氢元素的化合价为0;氢元素的化合价由+1价变为0价,化合价降低,H2O是氧化剂,被还原,发生了还原反应.
故答案为:Na.
点评 本题难度不大,掌握氧化还原反应中化学价升高的物质是还原剂、化学价降低的物质是氧化剂是正确解答本题的关键.

练习册系列答案
相关题目
11.根据图示信息和已学知识判断,下列说法正确的是( )
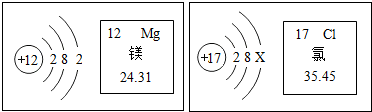

| A. | 镁原子核内有12个质子,最外层电子数是8 | |
| B. | 氯的相对原子质量为35.45 g,在化学变化中,氯原子易得电子 | |
| C. | 当X=8时,该微粒属于稀有气体元素的原子 | |
| D. | 镁离子(Mg2+)与氯离子(Cl-)的最外层电子数相等 |
15.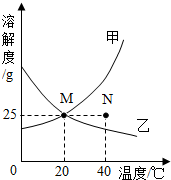 如图为甲、乙两种固体物质在水中的溶解度曲线.下列说法错误的是( )
如图为甲、乙两种固体物质在水中的溶解度曲线.下列说法错误的是( )
 如图为甲、乙两种固体物质在水中的溶解度曲线.下列说法错误的是( )
如图为甲、乙两种固体物质在水中的溶解度曲线.下列说法错误的是( )| A. | 甲、乙两物质都属于易溶物质 | |
| B. | 在20℃时,甲、乙两物质的溶解度相等 | |
| C. | 在40℃时,N点表示甲物质的不饱和溶液 | |
| D. | 在20℃时,乙物质的饱和溶液溶质质量分数为25% |
5.下列物质中蛋白质含量最高的是( )
| A. |  橙子 | B. |  大豆 | C. |  西红柿 | D. |  玉米 |
12.下列转化通过一步化学反应就能实现的是( )
| A. | CaCO3→Ca(OH)2 | B. | Cu→Ag | C. | NaCl→Na2CO3 | D. | KNO3→K2SO4 |
10. 小瑾同学用图表对所学知识进行归纳,其中甲包含乙和丙,不包含丁,下列关系错误的( )
小瑾同学用图表对所学知识进行归纳,其中甲包含乙和丙,不包含丁,下列关系错误的( )
 小瑾同学用图表对所学知识进行归纳,其中甲包含乙和丙,不包含丁,下列关系错误的( )
小瑾同学用图表对所学知识进行归纳,其中甲包含乙和丙,不包含丁,下列关系错误的( )| 甲 | 乙 | 丙 | 丁 | |
| A | 碱 | 烧碱 | 氢氧化钾 | 纯碱 |
| B | 有机物 | 甲烷 | 蛋白质 | 淀粉 |
| C | 溶液 | 糖水 | 生理盐水 | 泥浆 |
| D | 化石燃料 | 石油 | 煤 | 酒精 |
| A. | A | B. | B | C. | C | D. | D |
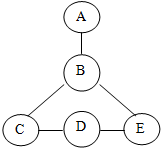 A~E均为初中化学中常见的物质,它们之间的关系如图所示,相互之间连线表示能发生化学反应.已知A和B反应时火星四射,C、D、E为不同类别的化合物,E的溶液为蓝色.回答下列问题:
A~E均为初中化学中常见的物质,它们之间的关系如图所示,相互之间连线表示能发生化学反应.已知A和B反应时火星四射,C、D、E为不同类别的化合物,E的溶液为蓝色.回答下列问题: