题目内容
9.一定温度时,将30g 硝酸钾放入100g水中,完全溶解,所得溶液中溶质的质量分数是23.1%;温度不变,在上述溶液中再加入30g 硝酸钾,有10g未能溶解,所得溶液中溶质的质量分数是33.3%,该温度下,硝酸钾的溶解度为50g/100g水;若将温度升高,10g未溶解的固体全部溶解,则所得溶液中溶质的质量分数是37.5%.分析 根据溶质质量分数=$\frac{溶质质量}{溶剂质量}$×100%计算溶质的质量分数,根据饱和溶液的溶质质量和溶剂质量的关系和溶解度得得含义计算溶解度.
解答 解:一定温度时,将30g 硝酸钾放入100g水中,完全溶解,所得溶液中溶质的质量分数是:$\frac{30g}{30g+100g}×100%$≈23.1%;
温度不变,在上述溶液中再加入30g 硝酸钾,有10g未能溶解,所得溶液中溶质的质量分数是:
$\frac{30g+30g-10g}{100g+30g+30g-10g}$×100%=33.3%,
由上述可知,在100g的水中溶解了50g硝酸钾达到了饱和状态,则该温度下,硝酸钾的溶解度为50g/100g水;
若将温度升高,10g未溶解的固体全部溶解,则所得溶液中溶质的质量分数是:
$\frac{30g+30g}{100g+30g+30g}$×100%=37.5%
故答为:23.1;33.3;50;37.5.
点评 本题难度不是很大,主要考查了有关溶液中溶质质量分数和溶解度的简单计算,从而加深学生对溶质质量分数和溶解度概念的理解,培养学生的计算能力和理解能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案
相关题目
11.二氧化氮是大气的污染物之一.煤燃烧会产生一部分二氧化氮气体,它会与空气中的氧气、水蒸气发生反应形成酸雨,NO2+O2+H2O═HNO3,配平后各物质的化学计量数分别是( )
| A. | 1,1,1,2 | B. | 2,1,1,2 | C. | 4,1,2,4 | D. | 6,2,3,6 |
4.下列关于水的认识的说法错误的是( )
| A. | 水是一种氧化物 | B. | 水是生命活动中不可缺少的物质 | ||
| C. | 水由氢分子和氧原子构成 | D. | 电解水时在负极得到氢气 |
14.将锌粒放入硫酸铜和硝酸银的溶液,充分反应,过滤,滤渣一定含有的金属是( )
| A. | 锌 | B. | 铜 | C. | 银 | D. | 银和铜 |
1.写出下列物质与氧气在点燃的条件下发生反应的现象及化学反应式
以上各反应均属于氧化反应也是化合反应.
| 事 例 | 观察到的现象 | 文字表达式 |
| 磷的燃烧 | 放热,有大量白烟 | |
| 木炭的燃烧 | ||
| 铁丝的燃烧 |
19.如图所示实验基本操作中正确的是( )
| A. |  | B. |  | C. |  | D. |  |
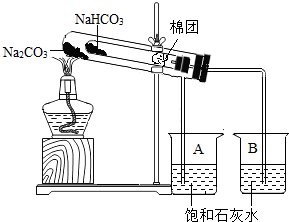 某校化学兴趣小组对苏打(Na2CO3)和小苏打(NaHCO3)在生活中具有何作用,如何鉴别苏打和小苏打进行了如下的探究实验活动,请你参与他们的探究过程,并回答相关问题:
某校化学兴趣小组对苏打(Na2CO3)和小苏打(NaHCO3)在生活中具有何作用,如何鉴别苏打和小苏打进行了如下的探究实验活动,请你参与他们的探究过程,并回答相关问题: