题目内容
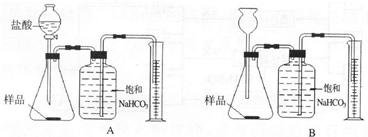
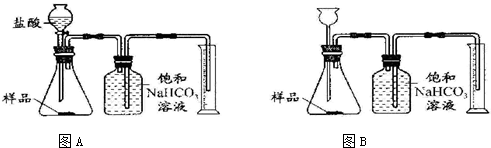
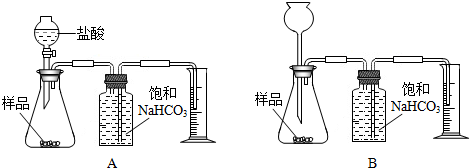
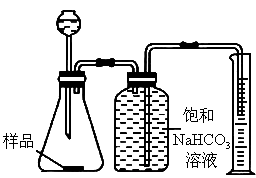
我国青海湖地区素有“夏天晒盐,冬天捞碱”之说,其中捞出的碱是碳酸钠和少量氯化钠的混合物.小王同学以捞出的碱作为样品,并用以下一套装置对样品进行分析,根据量筒中收集到的液体的体积
(相当于二氧化碳的体积)来计算样品中碳酸钠的含量.(已知:在饱和 溶液中基本不溶解)
溶液中基本不溶解)
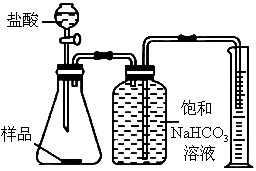
(1)
在A和B两套装置中,哪一套装置更合理______.(选填“A”或“B”)(2)
准确读取量筒内液体体积的方法是________________________.(3)
锥形瓶中原有的空气对实验结果是否有明显影响?__________.(填“有”或“没有”)(4)
若实验中用的盐酸是浓盐酸,则测得的样品中碳酸钠的含量与实际值相比会__________________.(填“偏大”、“偏小”或“不变”)(5)
在实验过程中,对取用样品的量的多少有一定要求,为什么?_________________________________________.
答案:略
解析:
解析:
|
(1)A (2) 取出导管,量筒平放,视线与溶液的凹液面的最低处相切(3) 没有(4) 偏大(5) 因为样品量太多会使液体外溢或气体外逸导致测量不准,太少会导致气体量太少,产生的气压不够,造成较大误差本题为实验题,主要涉及实验方案的设计、评价,能对具体实验操作过程中的问题进行讨论.本题的难点也正是在于具体实施某一实验方案时,需要考虑的实际影响因素、操作问题及其对实验结果造成的影响、改进的措施等.首先是装置的问题,由于是定量地测定样品中碳酸钠的含量,因此需对药品的量进行严格的控制,所以两套实验装置中使用分液漏斗的 A更符合要求.其次是实验操作的问题,读取量筒内液体时,由于导管直接插入了量筒中,因此必须先把导管从量筒中取出,再读数,否则读出的数据比实际偏大,影响最后的结果.同时,本题的实验方案在原理上是通过产生的二氧化碳排开饱和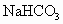 溶液的体积间接测量二氧化碳的体积,虽然空气中含有一定量的 溶液的体积间接测量二氧化碳的体积,虽然空气中含有一定量的 ,但含量在0.03%左右,相对于产生的 ,但含量在0.03%左右,相对于产生的 而言,可忽略不计.最后是使用药品的问题,浓盐酸因具有较强的挥发性,通常会挥发出氯化氢气体,根据题中所给信息, 而言,可忽略不计.最后是使用药品的问题,浓盐酸因具有较强的挥发性,通常会挥发出氯化氢气体,根据题中所给信息,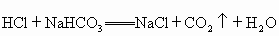 ,从而使测得的体积偏大. ,从而使测得的体积偏大. |

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目