题目内容
4.用扇子扇灭燃着的蜡烛,利用的主要灭火原理是( )| A. | 隔绝空气 | B. | 清除可燃物 | ||
| C. | 降低可燃物的着火点 | D. | 使可燃物温度降到着火点以下 |
分析 根据灭火的原理:清除或隔离可燃物、隔绝氧气或空气、使温度降到着火点以下,据此结合灭火方法进行分析判断.
解答 解:A、用扇子扇灭燃着的蜡烛,没有使蜡烛与空气隔绝,故选项错误.
B、除可燃物是把可燃物移走,而用扇子扇灭燃着的蜡烛没有移走蜡烛,没有清除可燃物,故选项错误.
C、着火点是物质本身的一种固有属性,一般不会改变,用扇子扇灭燃着的蜡烛没有降低蜡烛的着火点,故选项错误.
D、用扇子扇灭燃着的蜡烛,吹走了蜡烛火焰的热量,降低了蜡烛的温度,导致可燃物的温度降到了其着火点以下,故选项正确.
故选D.
点评 本题难度不大,考查灭火的原理,掌握灭火的原理并能灵活运用是正确解答此类题的关键.

练习册系列答案
相关题目
12.下列结论正确的是( )
| A. | 组成元素相同的物质其化学性质一定相同 | |
| B. | 化学反应中一定伴随能量的变化 | |
| C. | 饱和溶液降低温度一定会析出晶体 | |
| D. | 质子数相同的两种粒子其核外电子数一定相等 |
19.某化学实验活动小组的同学为了探究实验室中久置的氢氧化钠固体的成分,进行了有关实验,请你参与他们进行的探究活动:
【猜想与假设】
猜想Ⅰ:全部是NaOH;
猜想Ⅱ:全部是Na2CO3;
猜想Ⅲ:NaOH和Na2CO3.
【实验与探究】
(1)设计如下实验:
(2)为了进一步验证猜想结果,小明同学提出了如下实验方案:在完成步骤二的实验后,过滤,然后向滤液中滴加无色酚酞试液,若酚酞变红,则猜想Ⅲ成立;若酚酞不变红,则猜想Ⅱ成立.
小华同学立即对小明同学的方案提出了质疑,通过查阅资料知道:氯化钡溶液呈中性.因此氯化钡溶液不能使无色酚酞试液变红,但碳酸钠溶液呈碱性(填“酸”或“碱”),能使酚酞试液变红.所以,他认为该实验方案中应改进的是将氢氧化钡溶液改为加入过量的氯化钡溶液.
(3)实验小组的同学展开讨论,又提出了一个定量实验方案,通过测定产生沉淀的质量来证明猜想Ⅱ或Ⅲ成立.实验如下:准确称量m克固体样品于试管中,加入蒸馏水完全溶解,然后滴加足量氯化钙溶液,充分反应后过滤、洗涤、干燥称得沉淀的质量为n克,若猜想Ⅱ成立,则m与n的关系式为(用含m和n的等式或不等式表示,下同)n=$\frac{197m}{106}$;若猜想Ⅲ成立,则m与n的关系式又为n<$\frac{197m}{106}$.
【猜想与假设】
猜想Ⅰ:全部是NaOH;
猜想Ⅱ:全部是Na2CO3;
猜想Ⅲ:NaOH和Na2CO3.
【实验与探究】
| 实验操作步骤 | 实验现象 | 结论及解释 |
| 步骤一:取少量固体样品于试管中,加蒸馏水完全溶解,然后加入足量的稀盐酸. | 若实验过程中始终没有气泡产生. | 则证明猜想Ⅰ成立. |
| 步骤二:取少量固体样品于试管中,加蒸馏水完全溶解,然后滴加氢氧化钡溶液. | 若实验过程中产生白色沉淀. | 则证明猜想Ⅱ或Ⅲ成立,此过程中发生反应的化学方程式为Ba(OH)2+Na2CO3═BaCO3↓+2NaOH. |
(2)为了进一步验证猜想结果,小明同学提出了如下实验方案:在完成步骤二的实验后,过滤,然后向滤液中滴加无色酚酞试液,若酚酞变红,则猜想Ⅲ成立;若酚酞不变红,则猜想Ⅱ成立.
小华同学立即对小明同学的方案提出了质疑,通过查阅资料知道:氯化钡溶液呈中性.因此氯化钡溶液不能使无色酚酞试液变红,但碳酸钠溶液呈碱性(填“酸”或“碱”),能使酚酞试液变红.所以,他认为该实验方案中应改进的是将氢氧化钡溶液改为加入过量的氯化钡溶液.
(3)实验小组的同学展开讨论,又提出了一个定量实验方案,通过测定产生沉淀的质量来证明猜想Ⅱ或Ⅲ成立.实验如下:准确称量m克固体样品于试管中,加入蒸馏水完全溶解,然后滴加足量氯化钙溶液,充分反应后过滤、洗涤、干燥称得沉淀的质量为n克,若猜想Ⅱ成立,则m与n的关系式为(用含m和n的等式或不等式表示,下同)n=$\frac{197m}{106}$;若猜想Ⅲ成立,则m与n的关系式又为n<$\frac{197m}{106}$.
9.如图是电解水的微观模型示意图,从中获得的信息错误的是( )
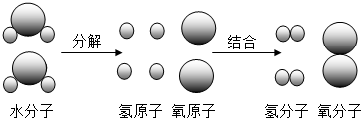

| A. | 反应前后物质的总质量没变 | |
| B. | 正负极上产生气体的质量比约为1:2 | |
| C. | 反应前后原子的种类和数目没有变化 | |
| D. | 在化学反应中分子可分而原子不可分 |
13.配制蔬菜的无土栽培营养液要用到KNO3做肥料,化肥KNO3是一种( )
| A. | 氮肥 | B. | 磷肥 | C. | 钾肥 | D. | 复合肥料 |
14.下列出去杂质的方法中,正确的是( )
| 选项 | 括号内为杂质 | 方法 |
| A | CO2(HCl) | 通过足量的NaOH溶液 |
| B | KCl(KClO3) | 加入少量MnO2加热 |
| C | NaCl(Na2CO3) | 加入足量的盐酸后蒸干 |
| D | Fe(Cu) | 加入足量的稀H2SO4后过滤 |
| A. | A | B. | B | C. | C | D. | D |