题目内容
在一些食品包装袋中放一些脱氧剂,可以除去袋中的氧气和水蒸气,从而使食品保质期延长.某校化学兴趣小组的同学为了探究脱氧剂的成分,打开小纸袋,将其倒在滤纸上,看到“脱氧剂”是灰黑色粉末,并混有少量的红色粉末.
【提出问题】该“脱氧剂”中的灰黑色、红色粉末各是什么?
【猜想】甲同学认为:灰黑色粉末为氧化铜、红色粉末为铜.
乙同学认为:灰黑色粉末为铁粉、红色粉末为氧化铁.
丙同学认为:灰黑色粉末为活性炭、红色粉末为氧化铁.
【设计方案】(1)证明乙同学猜想的实验方案如下:将得出的结论填写在下面的横线上
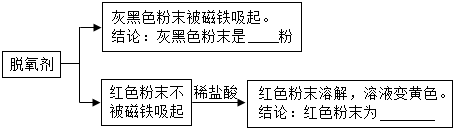
(2)根据实验结论可知铁与 和 接触易生锈.
(3)写出红色物质与稀盐酸反应的化学方程式 ;
(4)你认为能做食品脱氧剂的物质必须具备的性质(答两点) 、
.
(5)若铜中混有少量的氧化铜,请用两个不同类型的化学方程式表示除去氧化铜得到纯净的铜的方法 ; .
【提出问题】该“脱氧剂”中的灰黑色、红色粉末各是什么?
【猜想】甲同学认为:灰黑色粉末为氧化铜、红色粉末为铜.
乙同学认为:灰黑色粉末为铁粉、红色粉末为氧化铁.
丙同学认为:灰黑色粉末为活性炭、红色粉末为氧化铁.
【设计方案】(1)证明乙同学猜想的实验方案如下:将得出的结论填写在下面的横线上

(2)根据实验结论可知铁与
(3)写出红色物质与稀盐酸反应的化学方程式
(4)你认为能做食品脱氧剂的物质必须具备的性质(答两点)
(5)若铜中混有少量的氧化铜,请用两个不同类型的化学方程式表示除去氧化铜得到纯净的铜的方法
考点:实验探究物质的组成成分以及含量,常见金属的特性及其应用,金属锈蚀的条件及其防护,酸的化学性质,书写化学方程式、文字表达式、电离方程式
专题:科学探究
分析:(1)根据磁铁会吸引铁,溶液的显黄色进行分析;
(2)根据铁生锈的原理进行分析;
(3)根据(1)中的推断书写方程式;
(4)根据食品的要求进行分析;
(5)根据氢气具有还原性,能和氧化铜反应生成铜和水,氧化铜能和硫酸反应生成硫酸铜和水,而铜不能和硫酸反应进行解答.
(2)根据铁生锈的原理进行分析;
(3)根据(1)中的推断书写方程式;
(4)根据食品的要求进行分析;
(5)根据氢气具有还原性,能和氧化铜反应生成铜和水,氧化铜能和硫酸反应生成硫酸铜和水,而铜不能和硫酸反应进行解答.
解答:解:(1)磁铁会吸引灰色粉末,所以灰色粉末是铁粉,红色粉末不会被吸引,说明不是铁,和盐酸反应会生成黄色溶液,说明溶液中存在铁离子,红色粉末中存在+3价的铁,就是氧化铁,故答案为:铁;氧化铁;
(2)从实验中可以知道铁是吸收水和氧气后才转化成的氧化铁,故答案为:氧气;水;
(3)氧化铁和盐酸反应生成氯化铁和水,反应的化学方程式为Fe2O3+6HCl═2FeCl3+3H2O;故答案为:Fe2O3+6HCl═2FeCl3+3H2O;
(4)与食品接触的东西必须是无毒的,还得会除去氧气和水,不能与食品反应;故答案为:能与氧气和水反应、不与食品反应;
(5)氢气具有还原性,能和氧化铜反应生成铜和水,反应的化学方程式为H2+CuO
Cu+H2O;该反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,属于置换反应;氧化铜能和硫酸反应生成硫酸铜和水,而铜不能和硫酸反应,反应的方程式为CuO+H2SO4═CuSO4+H2O,该反应是两种化合物相互交换成分生成另外的两种化合物,属于复分解反应.故填:H2+CuO
Cu+H2O;CuO+H2SO4═CuSO4+H2O.
(2)从实验中可以知道铁是吸收水和氧气后才转化成的氧化铁,故答案为:氧气;水;
(3)氧化铁和盐酸反应生成氯化铁和水,反应的化学方程式为Fe2O3+6HCl═2FeCl3+3H2O;故答案为:Fe2O3+6HCl═2FeCl3+3H2O;
(4)与食品接触的东西必须是无毒的,还得会除去氧气和水,不能与食品反应;故答案为:能与氧气和水反应、不与食品反应;
(5)氢气具有还原性,能和氧化铜反应生成铜和水,反应的化学方程式为H2+CuO
| ||
| ||
点评:在解此类题时,首先根据题中的现象确定混合物的成分,然后再结合具体的问题结合学过的知识进行解答.

练习册系列答案
相关题目
关于电解水的过程,下列说法正确的是( )
| A、水分子数目不变 |
| B、水分子体积改变 |
| C、生成了新的原子 |
| D、生成了新的分子 |
 现有一瓶葡萄糖(C6H12O6)溶液,部分标签如图所示:请计算:(要求都写出计算过程)
现有一瓶葡萄糖(C6H12O6)溶液,部分标签如图所示:请计算:(要求都写出计算过程)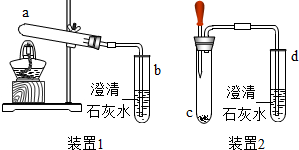 制作馒头时常加入泡打粉,在制作过程中由于产生二氧化碳气体,使馒头变得松软可口.小明对泡打粉的发面原理产生兴趣,进行了以下实验探究.
制作馒头时常加入泡打粉,在制作过程中由于产生二氧化碳气体,使馒头变得松软可口.小明对泡打粉的发面原理产生兴趣,进行了以下实验探究.

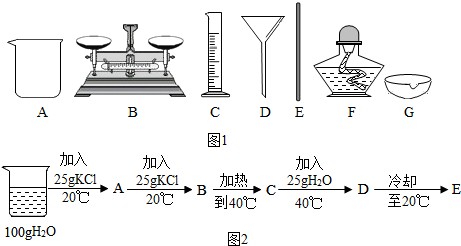
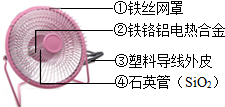 化学与我们的身体健康和生产生活有着密切的关系.
化学与我们的身体健康和生产生活有着密切的关系.