题目内容
10.能证明“CaCO3并非绝对不溶于水”的实验事实是( )| A. | 向少许CaCO3粉末加入NaOH溶液充分振荡,无明显现象 | |
| B. | 向少许CaCO3粉末加入3mL蒸馏水充分振荡,滴入酚酞试液即变红 | |
| C. | 向2颗蚕豆粒般石灰石固体加入3mL蒸馏水,滴入酚酞试液片刻内不变红 | |
| D. | 向少许CaCO3粉末加入过量稀盐酸充分振荡,粉末消失且有气泡产生 |
分析 A、根据CaCO3不与NaOH反应进行分析判断.
B、水显中性,不能使酚酞试液变红;少许CaCO3粉末加入3mL蒸馏水充分振荡,滴入酚酞试液即变红,说明存在碱性物质.
C、固体颗粒大小决定了固体与水的接触面积的大小,据此进行分析判断.
D、CaCO3能与稀盐酸反应产生气泡,与CaCO3是否溶于水无关.
解答 解:A、CaCO3不与NaOH溶液反应,向CaCO3粉末加入NaOH溶液充分振荡,无明显现象,不能证明“CaCO3并非绝对不溶于水”.故A错误;
B、水显中性,不能使酚酞试液变红;向少许CaCO3粉末加入3mL蒸馏水充分振荡,滴入酚酞试液即变红,说明是碳酸钙粉末能溶于水,显碱性,能证明“CaCO3并非绝对不溶于水”.故B正确;
C、由于石灰石固体与水接触面积小,即使能溶于水,片刻内溶解的量也很少,故加入3mL蒸馏水,滴入酚酞试液片刻内不变红,不能证明“CaCO3并非绝对不溶于水”.故C错误;
D、CaCO3能与稀盐酸反应,向少许CaCO3粉末加入过量稀盐酸充分振荡,粉末消失且有气泡产生,与CaCO3是否溶于水无关,不能证明“CaCO3并非绝对不溶于水”.故D错误;
故选:D.
点评 本题有一定难度,考查同学们灵活运用所学知识、化学实验方案设计与评价的能力,掌握碳酸钙的性质是正确解题的关键.

练习册系列答案
相关题目
20.下列各组离子在水中能大量共存的是( )
| A. | Na+、Ba2+、SO42- | B. | K+、NO3-、Cl- | C. | H+、Cu2+、OH- | D. | H+、CO32-、Cl- |
5.大力提倡“低碳生活”是我们每位公民的义务.“低碳生活”是指生活作息时所耗用能量要减少,从而减低碳特别是二氧化碳的排放.下列不属于“低碳生活”方式的是( )
| A. | 提倡大量使用无硫煤作燃料 | |
| B. | 短时间不用电脑时,关掉不用的程序,启用电脑的“睡眠”模式 | |
| C. | 多用永久性的筷子、饭盒,尽量避免使用一次性的餐具 | |
| D. | 多步行,骑自行车,尽量选用公共汽交通,少开车 |
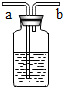 如图所示的装置有多种用途,请回答下列问题:
如图所示的装置有多种用途,请回答下列问题: