题目内容
13.下列物质量中氮元素的含量最高的是( )| A. | NO | B. | N2O3 | C. | NO2 | D. | N2O5 |
分析 各选项中都是氮的氧化物,先分别计算出N原子数为1的各物质的最简式,最简式中氧原子数越少,则其含氮量越高,据此进行解答.
解答 解:A.一氧化氮的分子式为NO,最简式为也是NO;
B.三氧化二氮的分子式为N2O3,最简式为${NO}_{\frac{3}{2}}$;
C.二氧化氮的分子式为NO2,最简式为NO2,
D.五氧化二氮的分子式为N2O5,最简式为${NO}_{\frac{5}{2}}$;
由于都是氮的氧化物,最简式中含有O原子数目越少,则其含氮量越高,所以含氮量最高的为一氧化氮,
故选A.
点评 本题考查了元素质量分数的计算,题目难度不大,注意掌握质量分数的概念及表达式,试题侧重基础知识的考查,培养了学生的化学计算能力.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
1.实验是学习化学的重要方法.以下关于实验的叙述中正确的是( )
| A. | 收集一集气瓶氢气,将带火星的木条放在集气瓶口验满 | |
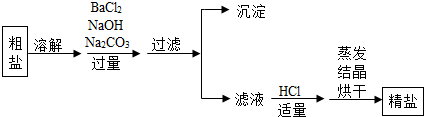
| B. | 粗盐提纯过滤盐水时,还要用玻璃棒轻轻搅动漏斗中的液体 | |
| C. | 某溶液中加入用盐酸酸化了的氯化钡溶液有白色沉淀生成,说明有硫酸根 | |
| D. | 检验装置的气密性要在加放试剂之前进行 |
5.下列物质都能电离出H+,其中不属于酸的是( )
| A. | HCl | B. | NaHSO4 | C. | H2SO4 | D. | HNO3 |
2.36某样品为铜和氧化铜的混合物,现对其进行成分分析,取10g此样品,向其中分五次加入稀硫酸,使之充分反应,每次所用稀硫酸的质量及剩余固体质量记于表:(反应化学方程式:
CuO+H2SO4═CuSO4+H2O,铜不参加反应)
试回答下列问题:
(1)10g样品中,氧化铜的质量为8g;
(2)10g样品中铜元素的质量总共为多少克?
(3)足量稀硫酸与10g此样品完全反应后,可生成多少克硫酸铜?
CuO+H2SO4═CuSO4+H2O,铜不参加反应)
| 第一次 | 第二次 | 第三次 | 第四次 | 第五次 | |
| 加入稀硫酸的质量(g) | 20 | 20 | 20 | 20 | 20 |
| 充分反应后剩余固体的质量(g) | 8 | 6 | 4 | 2 | 2 |
(1)10g样品中,氧化铜的质量为8g;
(2)10g样品中铜元素的质量总共为多少克?
(3)足量稀硫酸与10g此样品完全反应后,可生成多少克硫酸铜?
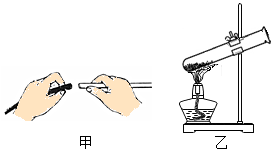 科学实验要注意正确的操作方法,否则会损坏仪器或带来安全威胁.
科学实验要注意正确的操作方法,否则会损坏仪器或带来安全威胁.