题目内容
现有①FeO;②Fe2O3;③Fe3O4;④FeS四种含铁化合物,其中含铁元素的质量分数由大到小的排列顺序是( )
| A、③>②>①>④ | B、①>③>②>④ | C、④>③>②>① | D、①>②>③>④ |
分析:要比较四种含铁的化合物中铁元素的质量分数大小,可以根据某元素的质量分数=
×100%先一一计算出每种化合物的中铁的质量分数,然后再进行比较其大小.
| 该元素的相对原子质量×其原子个数 |
| 化合物的相对分子质量 |
解答:解:①FeO铁元素的质量分数=
×100%≈77.8%;
②Fe2O3铁元素的质量分数=
×100%=70%
③Fe3O4铁元素的质量分数=
×100%=72.4%
④FeS铁元素的质量分数=
×100%=63.6%
根据计算可知铁元素的质量分数由大到小的排列顺序:①>③>②>④
故选:B
| 56 |
| 56+16 |
②Fe2O3铁元素的质量分数=
| 56×2 |
| 56×2+16×3 |
③Fe3O4铁元素的质量分数=
| 56×3 |
| 56×3+16×4 |
④FeS铁元素的质量分数=
| 56 |
| 56+32 |
根据计算可知铁元素的质量分数由大到小的排列顺序:①>③>②>④
故选:B
点评:本题是考查根据化学式通过计算比较铁元素的质量分数的大小,题目涉及的知识点比较单一,只要记住求元素的质量分数计算公式即可解答.

练习册系列答案
 优生乐园系列答案
优生乐园系列答案
相关题目
现有一包Fe和FeO的混合物,测得其中铁元素的质量分数为80%.取该混合物7.0g,加入100g9.8%稀硫酸恰好完全溶解,则生成溶液的溶质质量分数大约是( )
| A、14.2% | B、15.2% | C、15% | D、16.8% |
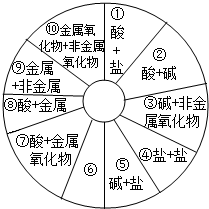 (2011?大庆)单质、氧化物、酸、碱、盐,这些不同类别的物质之间反应时都可以生成盐,现有同学构建了如图所示的知识网络图.
(2011?大庆)单质、氧化物、酸、碱、盐,这些不同类别的物质之间反应时都可以生成盐,现有同学构建了如图所示的知识网络图.